Δομή του οξειδίου του χρυσού (III) (Au2O3), ιδιότητες, ονοματολογία και χρήσεις
Το οξείδιο του χρυσού (III) είναι μια ανόργανη ένωση του οποίου ο χημικός τύπος είναι Au2Ο3. Θεωρητικά, κάποιος μπορεί να περιμένει τη φύση του να είναι ομοιοπολικού τύπου. Ωστόσο, η παρουσία ενός συγκεκριμένου ιοντικού χαρακτήρα στο στερεό του δεν μπορεί να απορριφθεί εντελώς. ή ό, τι είναι το ίδιο, υποθέστε την απουσία της άδειας3+ δίπλα στο ανιόν Ο2-.
Μπορεί να φαίνεται αντιφατικό ότι ο χρυσός, που είναι ευγενές μέταλλο, μπορεί να σκουριάσει. Υπό κανονικές συνθήκες, κομμάτια χρυσού (όπως τα αστέρια στην εικόνα παρακάτω) δεν μπορούν να οξειδωθούν με επαφή με οξυγόνο στην ατμόσφαιρα. Ωστόσο, όταν ακτινοβολείται με υπεριώδη ακτινοβολία παρουσία όζοντος, OR3, η εικόνα είναι διαφορετική.

Εάν τα χρυσά αστέρια υποστούν αυτές τις συνθήκες, θα μετατραπούν σε ένα κοκκινωπό καφέ, χαρακτηριστικό του Au2Ο3.
Άλλες μέθοδοι για την λήψη αυτού του οξειδίου θα συνεπάγονταν τη χημική επεξεργασία των εν λόγω αστεριών. για παράδειγμα, μετατροπή της χρυσού μάζας στο αντίστοιχο χλωρίδιο της, AuCl3.
Μετά, στο AuCl3, και τα υπόλοιπα πιθανά άλατα χρυσού που σχηματίζονται, προστίθεται ένα ισχυρό βασικό μέσον. και με αυτό, παίρνετε το ενυδατωμένο οξείδιο ή υδροξείδιο, Au (OH)3. Τέλος, αυτή η τελευταία ένωση θερμικώς αφυδατώνεται για να ληφθεί το Au2Ο3.
Ευρετήριο
- 1 Δομή του οξειδίου του χρυσού (III)
- 1.1 Ηλεκτρονικές πτυχές
- 1.2 Ενυδατώματα
- 2 Ιδιότητες
- 2.1 Φυσική εμφάνιση
- 2.2 Μοριακή μάζα
- 2.3 Πυκνότητα
- 2.4 Σημείο τήξης
- 2.5 Σταθερότητα
- 2.6 Διαλυτότητα
- 3 Ονοματολογία
- 4 Χρήσεις
- 4.1 Χρωματισμός γυαλιών
- 4.2 Σύνθεση αουριτών και χρυσαφένιο χρυσό
- 4.3 Χειρισμός αυτοσυναρμολογημένων μονοστοιβάδων
- 5 Αναφορές
Δομή του οξειδίου του χρυσού (III)
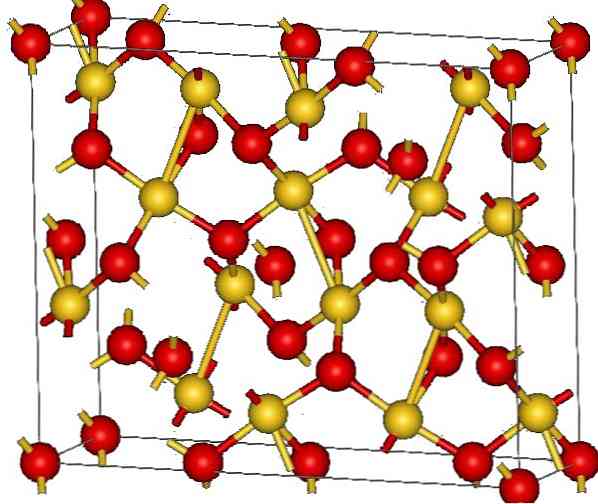
Η κρυσταλλική δομή του οξειδίου του χρυσού (III) φαίνεται στην επάνω εικόνα. Η διάταξη των ατόμων χρυσού και οξυγόνου στο στερεό δεικνύεται είτε ως ουδέτερα άτομα (ομοιοπολικά στερεά) είτε ως ιόντα (ιονικό στερεό). Είναι αλήθεια ότι αρκεί να εξαλείψουμε ή να τοποθετήσουμε τους συνδέσμους Au-O σε κάθε περίπτωση.
Σύμφωνα με την εικόνα, θεωρείται ότι επικρατεί ο ομοιοπολικός χαρακτήρας (ο οποίος θα ήταν λογικός). Για το λόγο αυτό, τα άτομα και οι δεσμοί που παρουσιάζονται παρουσιάζονται με σφαίρες και ράβδους, αντίστοιχα. Οι χρυσές σφαίρες αντιστοιχούν στα άτομα του χρυσού (AuIII-O) και κοκκινωπό σε άτομα οξυγόνου.
Αν κοιτάξετε προσεκτικά, θα δείτε ότι υπάρχουν μονάδες AuO4, τα οποία ενώνονται με άτομα οξυγόνου. Ένας άλλος τρόπος για να το απεικονίσετε θα ήταν να θεωρήσετε ότι κάθε Au3+ περιβάλλεται από τέσσερα O2-? Φυσικά, από ιονική άποψη.
Αυτή η δομή είναι κρυσταλλική επειδή τα άτομα διατάσσονται ακολουθώντας ένα ίδιο πρότυπο μεγάλης εμβέλειας. Έτσι, το μοναδιαίο κύτταρο του αντιστοιχεί στο ρομβοεδρικό κρυσταλλικό σύστημα (το ίδιο όπως στην άνω εικόνα). Ως εκ τούτου, όλα τα Au2Ο3 θα μπορούσε να κατασκευαστεί εάν όλες οι σφαίρες της μονάδας μονάδας διανεμήθηκαν στο διάστημα.
Ηλεκτρονικές πτυχές
Ο χρυσός είναι μεταβατικό μέταλλο και πρέπει να αναμένεται ότι τα 5d τροχιακά του αλληλεπιδρούν άμεσα με τα 2p τροχιακά του ατόμου οξυγόνου. Αυτή η επικάλυψη των τροχιακών τους θα πρέπει θεωρητικά να δημιουργεί ζώνες αγωγιμότητας, οι οποίες θα μετατρέπουν το Au2Ο3 σε ένα στερεό ημιαγωγό.
Επομένως, η πραγματική δομή του Au2Ο3 είναι ακόμη πιο πολύπλοκο με αυτό κατά νου.
Ενυδατώνει
Το οξείδιο του χρυσού μπορεί να συγκρατεί μόρια νερού μέσα στους ρομβοεδρικούς κρυστάλλους του, γεγονός που δημιουργεί ένυδρες μορφές. Όταν σχηματίζονται τέτοιες ένυδρες μορφές, η δομή γίνεται άμορφη, δηλαδή, διαταραγμένη.
Η χημική φόρμουλα για τέτοιες ενυδατωμένες ουσίες μπορεί να είναι οποιοδήποτε από τα ακόλουθα, τα οποία στην πραγματικότητα δεν είναι βαθιά αποσαφηνισμένα: Au2Ο3∙ zH2Ο (ζ = 1, 2, 3, κλπ.), Au (ΟΗ)3, ή AuxΟκαι(ΟΗ)z.
Ο τύπος Au (OH)3 αντιπροσωπεύει μια υπεραπλούστευση της πραγματικής σύνθεσης των εν λόγω ενυδατωμένων. Αυτό συμβαίνει επειδή στο χρυσό υδροξείδιο (III), οι ερευνητές έχουν βρει επίσης την παρουσία του Au2Ο3? και ως εκ τούτου, έχει νόημα να την αντιμετωπίζουμε μεμονωμένα ως ένα "απλό" υδροξείδιο μεταβατικού μετάλλου.
Από την άλλη πλευρά, ένα στερεό με τύπο AuxΟκαι(ΟΗ)z θα μπορούσε να αναμένεται μια άμορφη δομή. αφού αυτό εξαρτάται από τους συντελεστές x, και και z, οι παραλλαγές των οποίων θα δημιουργούσαν κάθε είδους δομή που δύσκολα θα μπορούσε να παρουσιάσει ένα κρυσταλλικό μοτίβο.
Ιδιότητες
Φυσική εμφάνιση
Είναι ένα κοκκινωπό καφέ στερεό.
Μοριακή μάζα
441,93 g / mol.
Πυκνότητα
11,34 g / mL.
Σημείο τήξης
Λιώνει και αποσυντίθεται στους 160ºC. Επομένως, δεν έχει σημείο βρασμού, οπότε αυτό το οξείδιο δεν φθάνει ποτέ στο σημείο βρασμού.
Σταθερότητα
Το Au2Ο3 είναι θερμοδυναμικώς ασταθής επειδή, όπως αναφέρθηκε στην αρχή, ο χρυσός δεν τείνει να οξειδώνεται κάτω από κανονικές συνθήκες θερμοκρασίας. Έτσι είναι εύκολα μειωμένη για να γίνει και πάλι ο ευγενής χρυσός.
Όσο υψηλότερη είναι η θερμοκρασία, τόσο ταχύτερη είναι η αντίδραση, η οποία είναι γνωστή ως θερμική αποσύνθεση. Έτσι, το Au2Ο3 στους 160 ° C αποσυντίθεται για να παράγει μεταλλικό χρυσό και απελευθερώνει μοριακό οξυγόνο:
2 Au2Ο3 => 4 Au + 3 O2
Μια πολύ παρόμοια αντίδραση μπορεί να συμβεί με άλλες ενώσεις που ευνοούν την εν λόγω μείωση. Γιατί μείωση; Επειδή ο χρυσός επιστρέφει για να κερδίσει τα ηλεκτρόνια που το οξυγόνο έβγαλε από αυτό. που είναι το ίδιο με το να λέει ότι χάνει δεσμούς με το οξυγόνο.
Διαλυτότητα
Είναι ένα στερεό αδιάλυτο στο νερό. Ωστόσο, είναι διαλυτό σε υδροχλωρικό οξύ και νιτρικό οξύ, λόγω του σχηματισμού χρυσών χλωριδίων και νιτρικών.
Ονοματολογία
Το οξείδιο του χρυσού (III) είναι το όνομα που διέπεται από την ονοματολογία των αποθεμάτων. Άλλοι τρόποι να αναφερθούν είναι:
-Παραδοσιακή ονοματολογία: οξυγόνο, επειδή το σθένος 3+ είναι το υψηλότερο για τον χρυσό.
-Συστηματική ονοματολογία: διόριο τριοξείδιο.
Χρησιμοποιεί
Χρωματισμός γυαλιών
Μια από τις πιο επιφανείς χρήσεις του είναι να παρέχει κοκκινωπά χρώματα σε ορισμένα υλικά, όπως τα γυαλιά, εκτός από την παροχή ορισμένων ιδιοτήτων εγγενών στα άτομα του χρυσού..
Σύνθεση αουριτών και χρυσαφένιο χρυσό
Εάν προστεθεί το Au2Ο3 σε ένα μέσο όπου είναι διαλυτό και παρουσία μετάλλων, οι αύρες μπορούν να καθιζάνουν μετά την προσθήκη μιας ισχυρής βάσης. τα οποία σχηματίζονται από ανιόντα AuO4- στην εταιρεία μεταλλικών κατιόντων.
Επίσης, το Au2Ο3 αντιδρά με την αμμωνία για να σχηματίσει τη χρυσή ορμητική ένωση, Au2Ο3(ΝΗ3)4. Το όνομά του προέρχεται από το γεγονός ότι είναι εξαιρετικά εκρηκτικό.
Χειρισμός αυτοσυναρμολογημένων μονοστιβάδων
Στον χρυσό και το οξείδιο του, ορισμένες ενώσεις, όπως διαλκυλ δισουλφίδια, RSSR, δεν απορροφώνται με τον ίδιο τρόπο. Όταν συμβαίνει αυτή η προσρόφηση, σχηματίζεται αυθόρμητα ένας Au-S δεσμός, όπου το άτομο θείου εμφανίζει και ορίζει τα χημικά χαρακτηριστικά της εν λόγω επιφάνειας ανάλογα με τη λειτουργική ομάδα με την οποία δεσμεύεται..
Το RSSR δεν μπορεί να προσροφηθεί στο Au2Ο3, αλλά σε μεταλλικό χρυσό. Επομένως, εάν τροποποιηθεί η επιφάνεια του χρυσού και ο βαθμός οξείδωσης του, καθώς και το μέγεθος των σωματιδίων ή των στρωμάτων του Au2Ο3, μπορεί να σχεδιαστεί μια πιο ετερογενής επιφάνεια.
Αυτή η επιφάνεια Au2Ο3-Το AuSR αλληλεπιδρά με τα μεταλλικά οξείδια ορισμένων ηλεκτρονικών συσκευών, αναπτύσσοντας έτσι πιο έξυπνες επιφάνειες.
Αναφορές
- Wikipedia. (2018). Οξείδιο του χρυσού (ΙΙΙ). Ανακτήθηκε από: en.wikipedia.org
- Χημική σύνθεση (2018). Χρυσό οξείδιο (III). Ανάκτηση από: formulacionquimica.com
- D. Michaud. (24 Οκτωβρίου 2016). Οξείδια του χρυσού. 911 Μεταλλουργός. Ανακτήθηκε από: 911metallurgist.com
- Shi, R. Asahi και C. Stampfl. (2007). Ιδιότητες των οξειδίων του χρυσού Au2Ο3 και Au2O: Διερεύνηση πρώτων αρχών. Η Αμερικανική Φυσική Εταιρεία.
- Cook, Kevin M. (2013). Οξείδιο του χρυσού ως στρώμα κάλυψης για χημεία επιφανειοδραστικών επιφανειών. Θέματα και Διατριβές. Βιβλίο 1460.


