Δομή του οξείδιο του αργύρου (Ag2O), ιδιότητες, ονοματολογία και χρήσεις
Το οξείδιο αργύρου είναι μια ανόργανη ένωση της οποίας η χημική φόρμουλα είναι Ag2Η δύναμη που ενώνει τα άτομα της είναι εντελώς ιοντικής φύσης. επομένως, αποτελείται από ένα ιοντικό στερεό όπου υπάρχει λόγος δύο κατιόντων Ag+ αλληλεπιδρώντας ηλεκτροστατικά με ένα ανιόν Ο2-.
Το ανιόν οξειδίου, Ο2-, προκύπτει από την αλληλεπίδραση των ατόμων αργύρου της επιφάνειας με το οξυγόνο του περιβάλλοντος. με πολύ παρόμοιο τρόπο με το σίδηρο και πολλά άλλα μέταλλα. Ένα ασημένιο κομμάτι ή κοσμήματα αντί για ερυθρότητα και καταρρέει σε σκουριά, γίνεται μαύρο, χαρακτηριστικό του οξειδίου του αργύρου.

Για παράδειγμα, στην παραπάνω εικόνα μπορείτε να δείτε ένα σκουριασμένο ασημένιο κύπελλο. Σημειώστε την μαυρισμένη επιφάνεια, αν και διατηρεί κάποια διακοσμητική λάμψη. γι 'αυτό και τα σκουριασμένα ασημένια αντικείμενα μπορούν να θεωρηθούν αρκετά ελκυστικά για διακοσμητικές χρήσεις.
Οι ιδιότητες του οξειδίου του αργύρου είναι τέτοιες που δεν καταστρέφουν, με την πρώτη ματιά, την αρχική μεταλλική επιφάνεια. Δημιουργείται σε θερμοκρασία δωματίου με απλή επαφή με το οξυγόνο στον αέρα. και ακόμα πιο ενδιαφέρον, μπορεί να αποσυντεθεί σε υψηλές θερμοκρασίες (πάνω από 200 ° C).
Αυτό σημαίνει ότι αν το ποτήρι της εικόνας κρατηθεί και η θερμότητα μιας έντονης φλόγας εφαρμοστεί, θα ανακτήσει την ασημένια λάμψη της. Επομένως, ο σχηματισμός της είναι μια θερμοδυναμικά αναστρέψιμη διαδικασία.
Το οξείδιο του αργύρου έχει και άλλες ιδιότητες και, πέρα από τον απλό τύπο του Ag2Ή περιλαμβάνει πολύπλοκες δομικές οργανώσεις και πλούσια ποικιλία στερεών ουσιών. Ωστόσο, ο Αγ2Ή ίσως, δίπλα στον Αγ2Ο3, το πιο αντιπροσωπευτικό των οξειδίων του αργύρου.
Ευρετήριο
- 1 Δομή οξείδιο αργύρου
- 1.1 Αλλαγές με τον αριθμό της βαλεντίας
- 2 Φυσικές και χημικές ιδιότητες
- 2.1 Μοριακό βάρος
- 2.2 Εμφάνιση
- 2.3 Πυκνότητα
- 2.4 Σημείο τήξης
- 2,5 Kps
- 2.6 Διαλυτότητα
- 2.7 Ομοιογενής χαρακτήρας
- 2.8 Αποσύνθεση
- 3 Ονοματολογία
- 3.1 Βαλένθια I και III
- 3.2 Συστηματική ονοματολογία για τα πολύπλοκα οξείδια του αργύρου
- 4 Χρήσεις
- 5 Αναφορές
Δομή του οξείδιο του αργύρου
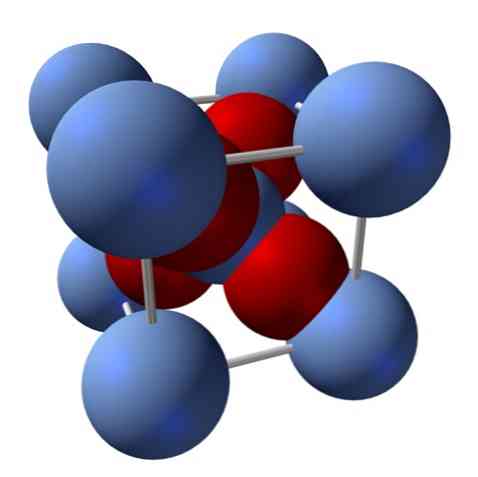
Πώς είναι η δομή του; Όπως αναφέρθηκε στην αρχή: είναι ένα ιοντικό στερεό. Για το λόγο αυτό, δεν μπορεί να υπάρχουν ομοιοπολικοί δεσμοί Ag - O ούτε Ag = O στη δομή του. αφού, αν υπήρχαν, οι ιδιότητες αυτού του οξειδίου θα αλλάζονταν δραστικά. Είναι τότε ιόντα Ag+ και Ο2- σε αναλογία 2: 1 και παρουσιάζει ηλεκτροστατική έλξη.
Η δομή του οξειδίου του αργύρου προσδιορίζεται κατά συνέπεια από τον τρόπο με τον οποίο οι ιοντικές δυνάμεις διαθέτουν στο χώρο τα ιόντα Ag+ και Ο2-.
Στην επάνω εικόνα, για παράδειγμα, έχετε μια κυψέλη μονάδας για ένα κυβικό κρυσταλλικό σύστημα: τα Ag cations+ είναι οι μπλε ασήμι σφαίρες, και το O2- τις κοκκινιστές σφαίρες.
Εάν υπολογίζετε τον αριθμό των σφαιρών, θα διαπιστώσετε ότι υπάρχουν, με την πρώτη ματιά, εννέα ασημί μπλε και τέσσερα κόκκινα χρώματα. Ωστόσο, λαμβάνονται υπόψη μόνο τα θραύσματα των σφαιρών που περιέχονται στον κύβο. της καταμέτρησης αυτών, ως κλάσματα των συνολικών σφαιρών, πρέπει να επιτευχθεί ο λόγος 2: 1 για τον Ag2Ο.
Επαναλαμβάνοντας τη δομική μονάδα του τετράεδρου AgO4 που περιβάλλεται από τέσσερις άλλους Αγ+, όλο το μαύρο στερεό είναι χτισμένο (αποφεύγοντας τα κενά ή τις ανωμαλίες που αυτές οι κρυστάλλινες ρυθμίσεις μπορούν να έχουν).
Αλλαγές με τον αριθμό της βαλεντίας
Εστιάζοντας τώρα όχι στο τετράεδρο AgO4 αλλά στη γραμμή AgOAg (παρατηρούμε τις κορυφές του ανώτερου κύβου), το στερεό οξείδιο του αργύρου αποτελείται, από μια άλλη οπτική γωνία, από πολλαπλές στοιβάδες ιόντων διατεταγμένες γραμμικά (αν και κεκλιμένες). Όλα αυτά ως αποτέλεσμα της "μοριακής" γεωμετρίας γύρω από τον Αγ+.
Τα παραπάνω επιβεβαιώνονται από αρκετές μελέτες της ιοντικής δομής του.
Το ασημένιο λειτουργεί κυρίως με σθένος +1, αφού όταν χάνει ένα ηλεκτρόνιο η προκύπτουσα ηλεκτρονική του διαμόρφωση είναι [Kr] 4d10, η οποία είναι πολύ σταθερή. Άλλα σθένη, όπως ο Αγ2+ και Ag3+ είναι λιγότερο σταθερές, καθώς χάνουν τα ηλεκτρόνια από τις τροχιές σχεδόν πλήρως γεμάτες.
Το ιόν Ag3+, Ωστόσο, είναι σχετικά λιγότερο ασταθές σε σύγκριση με τον Αγ2+. Στην πραγματικότητα, μπορεί να συνυπάρχει στην εταιρεία του Αγ+ Χημικώς εμπλουτίζει τη δομή.
Η ηλεκτρονική του διαμόρφωση είναι [Kr] 4δ8, με τα μη ζευγαρωμένα ηλεκτρόνια με τέτοιο τρόπο που να τους δίνει κάποια σταθερότητα.
Σε αντίθεση με τις γραμμικές γεωμετρίες γύρω από τα ιόντα Ag+, έχει βρεθεί ότι αυτή των ιόντων Ag3+ Είναι τετράγωνη επίπεδη. Ως εκ τούτου, ένα οξείδιο αργύρου με ιόντα Ag3+ θα αποτελείται από στρώματα που αποτελούνται από πλατείες AgO4 (όχι τετράεδρα) συνδεδεμένα ηλεκτροστατικά με γραμμές AgOAg. Αυτή είναι η περίπτωση του Αγ4Ο4 Ag2O ∙ Ag2Ο3 με μονοκλινική δομή.
Φυσικές και χημικές ιδιότητες

Εάν γρατσουνίζετε την επιφάνεια του ασημένιου κυπέλλου της κύριας εικόνας, θα πάρετε ένα στερεό, το οποίο δεν είναι μόνο μαύρο, αλλά έχει και καφέ ή καφέ τόνους (πάνω εικόνα). Μερικές από τις φυσικές και χημικές ιδιότητές του που αναφέρθηκαν από τις στιγμές είναι οι εξής:
Μοριακό βάρος
231,735 g / mol
Εμφάνιση
Στερεό μαύρο καφέ σε μορφή σκόνης (σημειώστε ότι παρά το γεγονός ότι είναι ιονικό στερεό, στερείται κρυσταλλικής εμφάνισης). Είναι άοσμο και αναμιγνύεται με νερό και δίνει μεταλλική γεύση
Πυκνότητα
7,14 g / mL.
Σημείο τήξης
277-300 ° C. Σίγουρα, λιώνει σε στερεό ασήμι. δηλαδή, πιθανώς διασπάται πριν σχηματιστεί υγρό οξείδιο.
Kps
1,52 ∙ 10-8 σε νερό στους 20 ° C. Είναι επομένως μια ένωση ελάχιστα διαλυτή στο νερό.
Διαλυτότητα
Αν κοιτάξετε προσεκτικά την εικόνα της δομής της, θα διαπιστώσετε ότι οι σφαίρες του Αγ2+ και Ο2- Δεν διαφωνούν σχεδόν σε μέγεθος. Ως αποτέλεσμα, μόνο μικρά μόρια μπορούν να διεισδύσουν στο εσωτερικό του κρυσταλλικού πλέγματος, καθιστώντας τα αδιάλυτα σε σχεδόν όλους τους διαλύτες. εκτός από εκείνες στις οποίες αντιδρά, όπως βάσεις και οξέα.
Ομοιογενής χαρακτήρας
Αν και έχει ειπωθεί επανειλημμένα ότι το οξείδιο του αργύρου είναι ιοντική ένωση, ορισμένες ιδιότητες, όπως το χαμηλό σημείο τήξης του, αντιβαίνουν σε αυτή τη δήλωση.
Βεβαίως, η εξέταση του ομοιοπολικού χαρακτήρα δεν καταρρέει αυτό που εξηγείται για τη δομή του, θα αρκούσε να το προσθέσουμε στη δομή του Ag2Ή ένα μοντέλο σφαιρών και ράβδων που υποδηλώνουν ομοιοπολικούς δεσμούς.
Επίσης, τα τετράεδρα και τα τετράγωνα επίπεδα AgO4, καθώς και οι γραμμές AgOAg, θα συνδεθούν με ομοιοπολικούς (ή ομοιοπολικούς ιοντικούς) δεσμούς.
Έχοντας αυτό υπόψη, ο Αγ2Ή θα ήταν στην πραγματικότητα ένα πολυμερές. Ωστόσο, συνιστάται να θεωρηθεί ως ένα ιοντικό στερεό με ομοιοπολικό χαρακτήρα (του οποίου η φύση του συνδέσμου εξακολουθεί να αποτελεί πρόκληση στις μέρες μας).
Αποσύνθεση
Αρχικά αναφέρθηκε ότι ο σχηματισμός της είναι θερμοδυναμικά αναστρέψιμος, έτσι απορροφά τη θερμότητα για να επιστρέψει στη μεταλλική της κατάσταση. Όλα αυτά μπορούν να εκφραστούν από δύο χημικές εξισώσεις για τέτοιες αντιδράσεις:
4Ag (s) + Ο2(g) => 2Ag2O (s) + Q
2Ag2O (s) + Q => 4Ag (s) + Ο2(ζ)
Όπου Q αντιπροσωπεύει τη θερμότητα στην εξίσωση. Αυτό εξηγεί γιατί η φωτιά που καίει την επιφάνεια του σκουριασμένου ασημένιου κυπέλλου επιστρέφει την ασημένια λάμψη της.
Επομένως, είναι δύσκολο να υποθέσουμε ότι υπάρχει Ag2O (l) δεδομένου ότι θα αποσυντεθεί άμεσα με θερμότητα. εκτός αν η πίεση είναι πολύ υψηλή για να ληφθεί το εν λόγω καφέ μαύρο υγρό.
Ονοματολογία
Όταν εισήχθη η δυνατότητα των ιόντων Ag2+ και Ag3+ εκτός από την κοινή και κυρίαρχη Αγ+, ο όρος «οξείδιο του αργύρου» αρχίζει να φαίνεται ανεπαρκής για να αναφερθεί στον Αγ2Ο.
Αυτό οφείλεται στο γεγονός ότι η Agion+ είναι πιο άφθονη από τις άλλες, οπότε ο Αγ παίρνει2Ή ως το μόνο οξείδιο. πράγμα που δεν είναι καθόλου σωστό.
Αν θεωρείτε ότι ο Αγ2+ ως πρακτικά ανύπαρκτο δεδομένης της αστάθειας του, τότε θα υπάρχουν μόνο τα ιόντα με σθένη +1 και +3. δηλαδή, Ag (Ι) και Ag (III).
Βαλένθια I και ΙΙΙ
Όντας ο Ag (I) το λιγότερο σθένος, ονομάζεται με την προσθήκη του επιθέματος -oso στο όνομά του argentum. Έτσι, ο Αγ2Ή είναι: το οξείδιο αργεντόζης ή, σύμφωνα με τη συστηματική ονοματολογία, το μονοξείδιο του διπλάτη.
Εάν το Αγ (ΙΙΙ) αγνοείται εντελώς, τότε η παραδοσιακή του ονοματολογία πρέπει να είναι: οξείδιο αργύρου αντί οξείδωσης αργεντινής.
Από την άλλη μεριά, το Ag (III) που είναι το μεγαλύτερο στέλεχος προστίθεται το suffix -ico στο όνομά του. Έτσι, ο Αγ2Ο3 είναι: οξείδιο αργύρου (2 ιόντα Ag)3+ με τρία O2-). Επίσης, το όνομά του σύμφωνα με τη συστηματική ονοματολογία θα είναι: τριοξείδιο του διπλάτη.
Εάν παρατηρηθεί η δομή του Ag2Ο3, μπορεί να θεωρηθεί ότι είναι το προϊόν της οξείδωσης από το όζον, Ή3, αντί του οξυγόνου. Συνεπώς, ο ομοιοπολικός χαρακτήρας του πρέπει να είναι μεγαλύτερος, καθώς είναι μια ομοιοπολική ένωση με δεσμούς Ag-O-O-O-Ag ή Ag-O.3-Ag.
Συστηματική ονοματολογία για σύνθετα οξείδια αργύρου
Το Αγ, που γράφτηκε επίσης ως Αγ4Ο4 Ag2O ∙ Ag2Ο3, είναι ένα οξείδιο αργύρου (I, III), καθώς έχει και τα δύο σθένη +1 και +3. Το όνομά του σύμφωνα με τη συστηματική ονοματολογία θα είναι: τετραπυλικό τετραπλό.
Αυτή η ονοματολογία είναι πολύ χρήσιμη όταν πρόκειται για άλλα στοιχειομετρικά πιο πολύπλοκα οξείδια αργύρου. Για παράδειγμα, υποθέστε τα δύο στερεά 2Ag2O ∙ Ag2Ο3 και Ag2O · 3Ag2Ο3.
Γράφοντας το πρώτο με έναν πιο κατάλληλο τρόπο θα ήταν: Αγ6Ο5 (καταμέτρηση και προσθήκη των ατόμων Ag και Ο). Το όνομά του θα ήταν τότε πεντοξείδιο εξαπλάτης. Σημειώστε ότι αυτό το οξείδιο έχει μια σύνθεση αργύρου λιγότερο πλούσια από την Ag2Ο (6: 5 < 2:1).
Ενώ γράφοντας το δεύτερο στερεό διαφορετικά, θα ήταν: Ag8Ο10. Το όνομά του θα ήταν το δεκαοξείδιο οκταπλάτης (με αναλογία 8:10 ή 4: 5). Αυτό το υποθετικό οξείδιο αργύρου θα ήταν "πολύ οξειδωμένο".
Χρησιμοποιεί
Μελέτες σε αναζήτηση νέων και περίπλοκων χρήσεων για οξείδιο του αργύρου εξακολουθούν να διεξάγονται σήμερα. Ορισμένες από τις χρήσεις του παρατίθενται παρακάτω:
-Διαλύεται σε αμμωνία, νιτρικό αμμώνιο και νερό για να σχηματίσει το αντιδραστήριο Tollens. Αυτό το αντιδραστήριο είναι ένα χρήσιμο εργαλείο για ποιοτικές αναλύσεις στα εργαστήρια οργανικής χημείας. Επιτρέπει τον προσδιορισμό της παρουσίας αλδεϋδών σε ένα δείγμα, ενώ η θετική απόκριση είναι ο σχηματισμός ενός «ασημί καθρέφτη» στο δοκιμαστικό σωλήνα.
-Μαζί με τον μεταλλικό ψευδάργυρο σχηματίζει τις πρωταρχικές μπαταρίες του οξειδίου ψευδαργύρου του αργύρου. Αυτή είναι ίσως μια από τις πιο κοινές και οικείες χρήσεις.
-Χρησιμεύει ως καθαριστής αερίου, απορροφώντας για παράδειγμα CO2. Όταν θερμαίνεται, απελευθερώνει τα παγιδευμένα αέρια και μπορεί να επαναχρησιμοποιηθεί αρκετές φορές.
-Λόγω των αντιμικροβιακών ιδιοτήτων του αργύρου, το οξείδιο του είναι χρήσιμο στις μελέτες βιοανάλυσης και καθαρισμού του εδάφους.
-Είναι ένας ήπιος παράγων οξειδώσεως ικανός να οξειδώνει αλδεϋδες προς καρβοξυλικά οξέα. Χρησιμοποιείται επίσης στην αντίδραση Hofmann (τριτοταγείς αμίνες) και συμμετέχει σε άλλες οργανικές αντιδράσεις, είτε ως αντιδραστήριο είτε ως καταλύτης.
Αναφορές
- Bergstresser Μ. (2018). Οξείδιο του αργύρου: Τύπος, αποσύνθεση και σχηματισμός. Μελέτη. Ανακτήθηκε από: study.com
- Συγγραφείς και συντάκτες των τόμων III / 17E-17F-41C. (s.f.). Οξείδια αργύρου (Ag (x) O (y)) κρυσταλλική δομή, παραμέτρους πλέγματος. (Αριθμητικά δεδομένα και λειτουργικές σχέσεις στην επιστήμη και την τεχνολογία), τόμος 41C. Springer, Βερολίνο, Χαϊδελβέργη.
- Η Μαχεράρα Κουμάρ Τριβέντι, ο Ράμα Μοχάν Ταλαπλαγκάντα, η Αλίκη Μπράντον, η Νάχριν Τριβέντι, ο Γκόπαλ Ναγιάκ, ο Ομπαράκης Λάιαλ, η Σνεχάις Τζάνα. (2015). Ο δυνητικός αντίκτυπος της ενεργειακής επεξεργασίας του βιολογικού πεδίου στις φυσικές και θερμικές ιδιότητες της σκόνης αργύρου οξείδιο. Διεθνές Περιοδικό Βιοϊατρικής Επιστήμης και Μηχανικής. Τόμος 3, Νο. 5, σελ. 62-68. doi: 10.11648 / j.ijbse.20150305.11
- Sullivan R. (2012). Αποσύνθεση του οξειδίου του αργύρου. Πανεπιστήμιο του Όρεγκον Ανακτήθηκε από: chemdemos.uoregon.edu
- Flint, Ντεϊάντα. (24 Απριλίου 2014). Χρήσεις μπαταριών αργιλίου-οξειδίου. Sciencing. Ανακτήθηκε από: sciencing.com
- Salman Montasir Ε. (2016). Μελέτη μερικών οπτικών ιδιοτήτων του οξείδιο του αργύρου (Ag2o) με τη χρήση φασματοφωτόμετρου UVVisible. [PDF] Ανακτήθηκε από: iosrjournals.org
- Bard Allen J. (1985). Βασικά δυναμικά σε υδατικό διάλυμα. Marcel Dekker. Ανακτήθηκε από: books.google.co.ve


