Θεωρία Μοντέλων και Παραδείγματα Ζώνης
Το θεωρία ζώνης είναι αυτή που ορίζει την ηλεκτρονική δομή του στερεού στο σύνολό του. Μπορεί να εφαρμοστεί σε οποιοδήποτε τύπο στερεού, αλλά είναι στα μέταλλα όπου αντανακλώνται οι μεγαλύτερες επιτυχίες του. Σύμφωνα με αυτή τη θεωρία, ο μεταλλικός δεσμός προκύπτει από την ηλεκτροστατική έλξη μεταξύ των θετικά φορτισμένων ιόντων και των κινητών ηλεκτρονίων στον κρύσταλλο.
Επομένως, ο μεταλλικός κρύσταλλος έχει "θάλασσα ηλεκτρονίων", που μπορεί να εξηγήσει τις φυσικές του ιδιότητες. Η κάτω εικόνα απεικονίζει τον μεταλλικό σύνδεσμο. Οι μωβ κουκκίδες των ηλεκτρονίων απομακρύνονται σε μια θάλασσα που περιβάλλει τα θετικά φορτισμένα μεταλλικά άτομα.

Η "θάλασσα των ηλεκτρονίων" σχηματίζεται από τις μεμονωμένες συνεισφορές κάθε ατόμου μετάλλου. Αυτές οι συνεισφορές είναι οι ατομικές τροχιές του. Οι μεταλλικές δομές είναι γενικά συμπαγείς. όσο πιο συμπαγή είναι, τόσο μεγαλύτερες είναι οι αλληλεπιδράσεις μεταξύ των ατόμων τους.
Ως αποτέλεσμα, τα ατομικά τους τροχιακά αλληλεπικαλύπτονται για να παράγουν πολύ στενά μοριακά τροχιακά στην ενέργεια. Η θάλασσα των ηλεκτρονίων είναι τότε μόνο μια μεγάλη σειρά μοριακών τροχιακών με διαφορετικές σειρές ενεργειών. Το εύρος αυτών των εντάσεων συνθέτει τις γνωστές ως ενεργειακές ζώνες.
Αυτές οι ζώνες υπάρχουν σε οποιαδήποτε περιοχή του κρυστάλλου, γι 'αυτό θεωρείται ως σύνολο, και από εκεί έρχεται ο ορισμός αυτής της θεωρίας.
Ευρετήριο
- 1 Μοντέλο ενεργειακών ζωνών
- 1.1 επίπεδο Fermi
- 2 Ημιαγωγοί
- 2.1 Εσωτερικοί και εξωγενείς ημιαγωγοί
- 3 Παραδείγματα εφαρμοζόμενης θεωρίας ζώνης
- 4 Αναφορές
Μοντέλο ενεργειακών ζωνών

Όταν το s τροχιακό ενός ατόμου μετάλλου αλληλεπιδρά με εκείνο του γείτονά του (N = 2), σχηματίζονται δύο μοριακά τροχιακά: ένας δεσμός (πράσινη ζώνη) και ένας δεσμός (σκούρα κόκκινη ζώνη).
Αν N = 3, τώρα σχηματίζονται τρία μοριακά τροχιακά, εκ των οποίων η μεσαία (μαύρη ζώνη) είναι μη δεσμευτική. Εάν N = 4, σχηματίζονται τέσσερα τροχιακά και το ένα με το μεγαλύτερο δεσμευτικό χαρακτήρα και το ένα με το μεγαλύτερο αντιψυκτικό χαρακτήρα χωρίζονται περαιτέρω.
Το φάσμα της διαθέσιμης ενέργειας για τα μοριακά τροχιακά αναπτύσσεται καθώς τα άτομα μετάλλων του κρυστάλλου παρέχουν τα τροχιακά τους. Αυτό έχει επίσης ως αποτέλεσμα τη μείωση του ενεργειακού χώρου μεταξύ των τροχιακών, στο σημείο που συμπυκνώνουν σε μια ζώνη.
Αυτή η μπάντα που αποτελείται από τροχιακά έχει περιοχές χαμηλής ενέργειας (εκείνες των πράσινων και κίτρινων χρωμάτων) και υψηλή ενέργεια (εκείνες των πορτοκαλί και κόκκινων χρωμάτων). Τα ενεργειακά άκρα τους έχουν χαμηλή πυκνότητα. Ωστόσο, τα περισσότερα από τα μοριακά τροχιακά (λευκή λωρίδα) συγκεντρώνονται στο κέντρο.
Αυτό σημαίνει ότι τα ηλεκτρόνια "τρέχουν πιο γρήγορα" μέσα από το κέντρο της μπάντας παρά στα άκρα τους.
Επίπεδο Fermi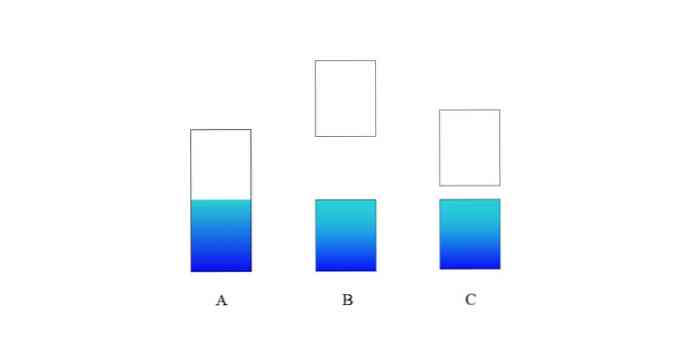
Είναι η υψηλότερη ενεργειακή κατάσταση που καταλαμβάνεται από τα ηλεκτρόνια σε ένα στερεό στην απόλυτη μηδενική θερμοκρασία (T = 0 K).
Μόλις κατασκευαστεί η μπάντα, τα ηλεκτρόνια αρχίζουν να καταλαμβάνουν όλες τις μοριακές τροχιές τους. Εάν το μέταλλο έχει ένα μόνο (α)1), όλα τα ηλεκτρόνια του κρυστάλλου του θα καταλάβουν το ήμισυ της μπάντας.
Το άλλο μη κατειλημμένο μισό είναι γνωστό ως οδηγώντας μπάντα, ενώ η μπάντα γεμάτη ηλεκτρόνια ονομάζεται ζώνη σθένους.
Στην επάνω εικόνα το Α αντιπροσωπεύει μία τυπική ζώνη σθένους (μπλε) και μια ταινία αγωγιμότητας (λευκό) για ένα μέταλλο. Η γαλαζωπή γραμμή συνόρων δείχνει το επίπεδο του Fermi.
Επειδή τα μέταλλα έχουν επίσης p-τροχιακά, συνδυάζουν με τον ίδιο τρόπο την προέλευση ενός p-band (λευκό).
Στην περίπτωση των μετάλλων, οι ζώνες s και p είναι πολύ κοντά στην ενέργεια. Αυτό επιτρέπει τις αλληλεπικαλύψεις τους, προάγοντας τα ηλεκτρόνια από τη ζώνη σθένους στη ζώνη αγωγιμότητας. Αυτό συμβαίνει ακόμη και σε θερμοκρασίες λίγο πάνω από 0 K.
Για τα μεταβατικά μέταλλα και από την περίοδο 4 προς τα κάτω, είναι επίσης δυνατό να σχηματιστούν ζώνες.
Το επίπεδο Fermi σε σχέση με τη ζώνη αγωγιμότητας είναι πολύ σημαντικό για τον προσδιορισμό των ηλεκτρικών ιδιοτήτων.
Για παράδειγμα, ένα μέταλλο Z με επίπεδο Fermi πολύ κοντά στη ζώνη αγωγιμότητας (η πλησιέστερη κενή ζώνη στην ενέργεια) έχει υψηλότερη ηλεκτρική αγωγιμότητα από ένα μέταλλο Χ στο οποίο το επίπεδο του Fermi είναι πολύ μακριά από αυτή τη ζώνη..
Ημιαγωγοί
Η ηλεκτρική αγωγιμότητα στη συνέχεια αποτελείται από τη μετανάστευση ηλεκτρονίων από μια ζώνη σθένους σε μια ζώνη αγωγιμότητας.
Αν το ενεργειακό χάσμα μεταξύ των δύο ζωνών είναι πολύ μεγάλο, έχουμε ένα μονωτικό στερεό (όπως με το Β). Από την άλλη πλευρά, αν το κενό είναι σχετικά μικρό, το στερεό είναι ημιαγωγός (στην περίπτωση του C).
Αντιμέτωποι με αύξηση της θερμοκρασίας, τα ηλεκτρόνια στη ζώνη σθένους αποκτούν αρκετή ενέργεια για να μεταναστεύσουν προς τη ζώνη αγωγιμότητας. Αυτό έχει ως αποτέλεσμα ένα ηλεκτρικό ρεύμα.
Στην πραγματικότητα, πρόκειται για μια ποιότητα υλικών στερεών ή ημιαγωγών: σε θερμοκρασία δωματίου είναι μονωτήρες, αλλά σε υψηλές θερμοκρασίες είναι αγωγοί.
Εγγενείς και εξωγενείς ημιαγωγοί

Οι εγγενείς αγωγοί είναι εκείνοι στους οποίους το ενεργειακό χάσμα μεταξύ της ζώνης σθένους και της ζώνης αγωγιμότητας είναι αρκετά μικρό ώστε η θερμική ενέργεια να επιτρέπει τη διέλευση των ηλεκτρονίων.
Από την άλλη πλευρά, οι εξωτερικοί αγωγοί εμφανίζουν μεταβολές στις ηλεκτρονικές τους δομές μετά από ντόπινγκ με ακαθαρσίες, οι οποίες αυξάνουν την ηλεκτρική τους αγωγιμότητα. Αυτή η ακαθαρσία μπορεί να είναι ένα άλλο μέταλλο ή ένα μη μεταλλικό στοιχείο.
Εάν η ακαθαρσία έχει περισσότερα ηλεκτρόνια σθένους, μπορεί να παρέχει μια ζώνη δότη που χρησιμεύει ως γέφυρα για να διασχίσουν τα ηλεκτρόνια της ζώνης σθένους στη ζώνη αγωγιμότητας. Αυτά τα στερεά είναι ημιαγωγοί τύπου η. Εδώ ο χαρακτηρισμός n προέρχεται από το "αρνητικό".
Στην επάνω εικόνα η ζώνη δότη απεικονίζεται στο μπλε μπλοκ ακριβώς κάτω από την ταινία οδήγησης (Τύπος n).
Από την άλλη πλευρά, εάν η πρόσμειξη έχει λιγότερα ηλεκτρόνια σθένους, παρέχει μια ζώνη δέκτη, η οποία συντομεύει το ενεργειακό χάσμα μεταξύ της ζώνης σθένους και της ζώνης οδήγησης..
Τα πρώτα ηλεκτρόνια μετακινούνται προς αυτή τη ζώνη, αφήνοντας πίσω τους «θετικές οπές», οι οποίες κινούνται προς την αντίθετη κατεύθυνση.
Καθώς αυτά τα θετικά κενά σημαίνουν τη διέλευση των ηλεκτρονίων, το στερεό ή το υλικό είναι ημιαγωγός τύπου ρ..
Παραδείγματα εφαρμοσμένης θεωρίας ζώνης
- Εξηγήστε γιατί τα μέταλλα είναι φωτεινά: τα κινητά τους ηλεκτρόνια μπορούν να απορροφήσουν την ακτινοβολία σε ένα ευρύ φάσμα μήκους κύματος όταν πηδούν σε υψηλότερα επίπεδα ενέργειας. Στη συνέχεια εκπέμπουν φως, επιστρέφοντας στα χαμηλότερα επίπεδα της κινητήριας ζώνης.
- Το κρυσταλλικό πυρίτιο είναι το πιο σημαντικό υλικό ημιαγωγών. Αν ένα τμήμα πυριτίου είναι εφοδιασμένο με ίχνη ενός στοιχείου ομάδας 13 (Β, ΑΙ, Ga, In, ΤΙ), γίνεται ημιαγωγός τύπου ρ. Ενώ εάν είναι ντοπαρισμένο με ένα στοιχείο της ομάδας 15 (N, P, As, Sb, Bi) γίνεται ημιαγωγός τύπου η.
- Η δίοδος εκπομπής φωτός (LED) είναι ένας ημιαγωγός p-n. Τι εννοείς; Ότι το υλικό έχει και τους δύο τύπους ημιαγωγών, τόσο το n όσο και το p. Τα ηλεκτρόνια μετακινούνται από τη ζώνη αγωγιμότητας του ημιαγωγού τύπου η, στη ζώνη σθένους του ημιαγωγού τύπου ρ.
Αναφορές
- Whitten, Davis, Peck & Stanley. Χημεία (8η έκδοση). CENGAGE Learning, σελ. 486-490.
- Shiver & Atkins. (2008). Ανόργανη χημεία (Τέταρτη έκδοση, σελ. 103-107, 633-635). Mc Graw Hill.
- Σκάφος C. R. (2016). Θεωρία ταινιών των στερεών. Ανακτήθηκε στις 28 Απριλίου 2018, από: hyperphysics.phy-astr.gsu.edu
- Steve Kornic (2011). Πηγαίνοντας από ομόλογα σε συγκροτήματα από την οπτική γωνία του χημικού. Ανακτήθηκε στις 28 Απριλίου 2018, από: chembio.uoguelph.ca
- Wikipedia. (2018). Εξωγενής ημιαγωγός. Ανακτήθηκε στις 28 Απριλίου 2018, από: en.wikipedia.org
- BYJU'S. (2018). Θεωρία ζωνών των μετάλλων. Ανακτήθηκε στις 28 Απριλίου 2018, από: byjus.com



