Αιθέρες αιθέρα, δομή, απόκτηση, χρήσεις
Το αιθυλαιθέρα, επίσης γνωστή ως διαιθυλαιθέρας, είναι μια οργανική ένωση της οποίας ο χημικός τύπος είναι C4H10O. Χαρακτηρίζεται από το ότι είναι ένα άχρωμο και πτητικό υγρό και συνεπώς τα μπουκάλια του πρέπει να διατηρούνται κλειστά όσο το δυνατόν ερμητικά.
Ο αιθέρας αυτός κατατάσσεται ως μέλος των διαλκυλ αιθέρων. δηλαδή, έχουν τον τύπο ROR ', όπου τα R και R' αντιπροσωπεύουν διαφορετικά τμήματα άνθρακα. Και καθώς περιγράφει το μεσαίο του όνομα, ο διαιθυλαιθέρας είναι δύο ρίζες-αιθύλιο εκείνες που δεσμεύονται στο άτομο οξυγόνου.

Αρχικά χρησιμοποιήθηκε αιθυλαιθέρας ως γενικό αναισθητικό, το οποίο εισήχθη το 1846 από τον William Thomas Green Morton. Ωστόσο, λόγω της ευφλεκτότητάς του, η χρήση της απορρίφθηκε, αντικαθιστώντας την με άλλα λιγότερο επικίνδυνα αναισθητικά..
Αυτή η ένωση έχει επίσης χρησιμοποιηθεί για την εκτίμηση του χρόνου κυκλοφορίας του αίματος, κατά την αξιολόγηση της καρδιαγγειακής κατάστασης των ασθενών.
Εντός του σώματος, ο διαιθυλαιθέρας μπορεί να μετασχηματιστεί σε διοξείδιο του άνθρακα και μεταβολίτες. τα τελευταία καταλήγουν να εκκρίνονται στα ούρα. Ωστόσο, το μεγαλύτερο μέρος του χορηγούμενου αιθέρα εκπνέεται στους πνεύμονες, χωρίς να υποβάλλονται σε καμία τροποποίηση.
Από την άλλη πλευρά, χρησιμοποιείται ως διαλύτης για σαπούνια, έλαια, αρώματα, αλκαλοειδή και κόμμεα.
Ευρετήριο
- 1 Δομή αιθυλαιθέρα
- 1.1 Διαμοριακές δυνάμεις
- 2 Φυσικές και χημικές ιδιότητες
- 2.1 Άλλα ονόματα
- 2.2 Μοριακός τύπος
- 2.3 Μοριακό βάρος
- 2.4 Φυσική εμφάνιση
- 2.5 Οσμή
- 2.6 Γεύση
- 2.7 Σημείο ζέσεως
- 2.8 Σημείο τήξης
- 2.9 Σημείο ανάφλεξης
- 2.10 Διαλυτότητα στο νερό
- 2.11 Διαλυτότητα σε άλλα υγρά
- 2.12 Πυκνότητα
- 2.13 Πυκνότητα ατμών
- 2.14 Πίεση ατμών
- 2.15 Σταθερότητα
- 2.16 Αυτόματη ανάφλεξη
- 2.17 Αποσύνθεση
- 2.18 Ιξώδες
- 2.19 Θερμότητα καύσης
- 2.20 Θερμοκρασία εξάτμισης
- 2.21 Επιφανειακή τάση
- 2.22 Δυναμικό ιονισμού
- 2.23 Όριο οσμής
- 2.24 Δείκτης διάθλασης
- 3 Λήψη
- 3.1 Από την αιθυλική αλκοόλη
- 3.2 Από το αιθυλένιο
- 4 Τοξικότητα
- 5 Χρήσεις
- 5.1 Οργανικός διαλύτης
- 5.2 Γενική αναισθησία
- 5.3 Πνεύμα του αιθέρα
- 5.4 Αξιολόγηση της κυκλοφορίας του αίματος
- 5.5 Εργαστήρια διδασκαλίας
- 6 Αναφορές
Δομή αιθυλαιθέρα
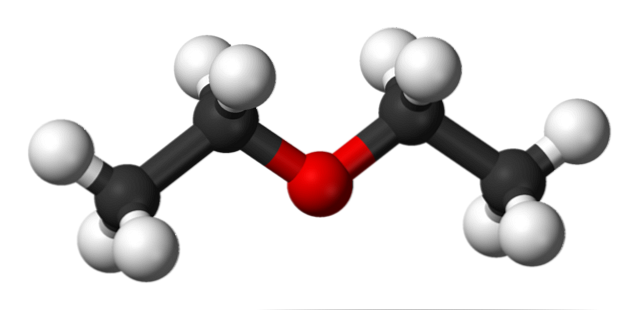
Στην παραπάνω εικόνα έχουμε μια αναπαράσταση με ένα μοντέλο σφαιρών και ράβδων της μοριακής δομής του αιθυλαιθέρα.
Όπως μπορεί να φανεί, η κόκκινη σφαίρα, που αντιστοιχεί στο άτομο οξυγόνου, έχει δύο ομάδες αιθυλίου συνδεδεμένες και στις δύο πλευρές. Όλοι οι σύνδεσμοι είναι απλοί, εύκαμπτοι και ελεύθερα περιστρεφόμενοι γύρω από τους άξονες σ.
Αυτές οι περιστροφές προέρχονται από στερεοϊσομερή γνωστά ως διαμορφομερή. ότι περισσότερο από ισομερή, είναι εναλλακτικά χωρικά κράτη. Η δομή της εικόνας αντιστοιχεί ακριβώς στον αντιμορφοποιητή, στον οποίο όλες οι ομάδες των ατόμων είναι κλιμακωτές (χωρισμένες μεταξύ τους).
Ποιος θα είναι ο άλλος διαμορφωτής; Η έκλειψη και αν και η εικόνα σας δεν είναι διαθέσιμη, απλώς την απεικονίστε με σχήμα U. Στα επάνω άκρα του U θα βρίσκονται οι ομάδες μεθυλίου, -CH3, που θα είχαν στερικές αντιδράσεις (θα συγκρούονταν στο διάστημα).
Ως εκ τούτου, αναμένεται ότι το μόριο CH3CH2OCH2CH3 υιοθετήσουν την αντιδιαμόρφωση τις περισσότερες φορές.
Διαμοριακές δυνάμεις
Με ποιες διαμοριακές δυνάμεις είναι τα μόρια του αιθυλαιθέρα που διέπονται στην υγρή φάση; Διατηρούνται στο υγρό κυρίως χάρη στις δυνάμεις διασποράς, καθώς η διπολική τους στιγμή (1.5D) στερείται επαρκώς ανεπαρκούς περιοχής ηλεκτρονικής πυκνότητας (δ +)
Αυτό συμβαίνει επειδή κανένα άτομο άνθρακα των ομάδων αιθυλίου δεν δίνει υπερβολική πυκνότητα ηλεκτρονίων στο άτομο οξυγόνου. Τα παραπάνω είναι προφανή με το χάρτη του ηλεκτροστατικού δυναμικού του αιθυλαιθέρα στο χέρι (κάτω εικόνα). Σημειώστε την απουσία μπλε περιοχής.
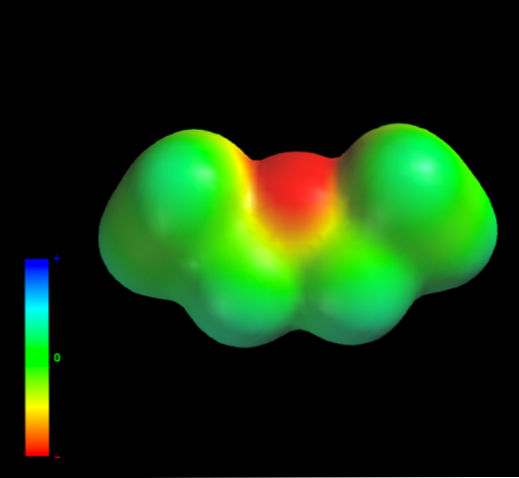
Το οξυγόνο δεν μπορεί να σχηματίσει δεσμούς υδρογόνου, και πάλι, επειδή δεν υπάρχουν διαθέσιμοι δεσμοί Ο-Η στη μοριακή δομή. Επομένως, τα στιγμιαία δίπολα και η μοριακή τους μάζα ευνοούν τις δυνάμεις διασποράς τους.
Παρ 'όλα αυτά, είναι πολύ διαλυτό στο νερό. Γιατί; Επειδή το άτομο του οξυγόνου, με μεγαλύτερη πυκνότητα ηλεκτρονίων, μπορεί να δέχεται δεσμούς υδρογόνου από ένα μόριο νερού:
(CH3CH2)2Οδ- - δ+Η-ΟΗ
Αυτές οι αλληλεπιδράσεις ευθύνονται για 6,04 g αυτού του αιθέρα που διαλύεται σε 100 ml νερού.
Φυσικές και χημικές ιδιότητες
Άλλα ονόματα
-Διαιθυλαιθέρας
-Αιθοξυαιθάνιο
-Αιθυλοξείδιο
Μοριακός τύπος
Γ4H10Ο ή (C2H5)2Ο.
Μοριακό βάρος
74,14 g / mol.
Φυσική εμφάνιση
Άχρωμο υγρό.
Οσμή
Γλυκό και πικάντικο.
Γεύση
Καίγοντας και γλυκό.
Σημείο ζέσεως
94,3 ° F (34,6 ° C) έως 760 mmHg.
Σημείο τήξης
-177,3 ° F (-116,3 ° C). Σταθερά κρύσταλλα.
Σημείο ανάφλεξης
-49ºF (κλειστός περιέκτης).
Διαλυτότητα στο νερό
6,04 g / 100mL στους 25 ° C.
Διαλυτότητα σε άλλα υγρά
Αναμείξιμο με αλειφατικές αλκοόλες βραχείας αλυσίδας, βενζόλιο, χλωροφόρμιο, πετρελαϊκό αιθέρα, διαλύτη λίπους, πολλά έλαια και πυκνό υδροχλωρικό οξύ.
Διαλυτό σε ακετόνη και πολύ διαλυτό σε αιθανόλη. Είναι επίσης διαλυτό σε νάφθα, βενζόλιο και έλαια.
Πυκνότητα
0,714 mg / mL στους 68 ° F (20 ° C).
Πυκνότητα ατμών
2,55 (σε σχέση με τον αέρα που λαμβάνεται με πυκνότητα 1).
Πίεση ατμού
442 mmHg στους 68 ° F. 538 mmHg στους 25 ° C. 58,6 kPa στους 20 ° C.
Σταθερότητα
Αργότερα οξειδώνεται με τη δράση του αέρα, της υγρασίας και του φωτός με το σχηματισμό υπεροξειδίων.
Ο σχηματισμός υπεροξειδίων μπορεί να συμβεί σε δοχεία αιθέρα που έχουν ανοιχθεί και παραμένουν σε αποθήκη για περισσότερο από έξι μήνες. Τα υπεροξείδια μπορούν να εκραγούν με τριβή, κρούση ή θέρμανση.
Αποφύγετε την επαφή με: ψευδάργυρο, αλογόνα, μη μεταλλικά οξυαλογονίδια, ισχυρά οξειδωτικά μέσα, χρώμιο χλωρίδιο, έλαια τεμεντίνης, νιτρικά και χλωριούχα μέταλλα.
Αυτόματη ανάφλεξη
356 ° F (180 ° C).
Αποσύνθεση
Όταν θερμαίνεται, αποσυντίθεται, εκπέμποντας ένα πικάντικο και ερεθιστικό καπνό.
Ιξώδες
0.2448 cPoise στους 20 ° C.
Θερμότητα καύσης
8,807 Kcal / g.
Θερμοκρασία εξάτμισης
89,8 cal / g στους 30 ° C.
Επιφανειακή τάση
17.06 dynes / cm στους 20 ° C.
Δυναμικό ιονισμού
9.53 eV.
Όριο οσμής
0,83 ppm (η καθαρότητα δεν δίνεται).
Δείκτης διάθλασης
1,355 στους 15 ºC.
Λήψη
Από την αιθυλική αλκοόλη
Ο αιθυλαιθέρας μπορεί να ληφθεί από αιθυλική αλκοόλη, παρουσία θειικού οξέος ως καταλύτη. Το θειικό οξύ σε ένα υδατικό μέσο διαχωρίζει την παραγωγή του ιόντος υδρογόνου, Η3Ο+.
Η άνυδρη αιθυλική αλκοόλη ρέει διαμέσου του διαλύματος θειικού οξέος, που θερμαίνεται μεταξύ 130 ° C και 140 ° C, παράγοντας την πρωτονίωση μορίων αιθυλικής αλκοόλης. Στη συνέχεια, ένα άλλο μόριο μη πρωτονιωμένης αιθυλικής αλκοόλης αντιδρά με το πρωτονιωμένο μόριο.
Όταν συμβαίνει αυτό, η πυρηνόφιλη προσβολή του δεύτερου μορίου αιθυλικής αλκοόλης προωθεί την απελευθέρωση νερού από το πρώτο μόριο (το πρωτονιωμένο). ως αποτέλεσμα, σχηματίζεται πρωτονιωμένος αιθυλαιθέρας (CH3CH2ΟΗΟΗ2CH3), με μερικώς φορτισμένο οξυγόνο θετικό.
Ωστόσο, αυτή η μέθοδος σύνθεσης χάνει την αποδοτικότητα επειδή το θειικό οξύ αραιώνεται με το νερό που παράγεται στη διαδικασία (προϊόν της αφυδάτωσης της αιθυλικής αλκοόλης).
Η θερμοκρασία της αντίδρασης είναι κρίσιμη. Σε θερμοκρασίες κάτω από τους 130 ° C, η αντίδραση είναι αργή και, ως επί το πλείστον, η αιθυλική αλκοόλη θα αποσταχθεί.
Πάνω από 150 ° C, το θειικό οξύ προκαλεί το σχηματισμό αιθυλενίου (το αλκένιο διπλού δεσμού), αντί να συνδυάζεται με αιθυλική αλκοόλη για να σχηματίσει αιθυλαιθέρα.
Από το αιθυλένιο
Στην αντίθετη διαδικασία, δηλαδή την ενυδάτωση του αιθυλενίου στη φάση ατμού, μπορεί να σχηματιστεί αιθυλαιθέρας ως παραπροϊόν εκτός από την αιθυλική αλκοόλη. Στην πραγματικότητα, αυτή η συνθετική οδός παράγει το μεγαλύτερο μέρος αυτής της οργανικής ένωσης.
Αυτή η διαδικασία χρησιμοποιεί καταλύτες φωσφορικού οξέος σταθεροποιημένους σε ένα στερεό υπόστρωμα, που είναι σε θέση να προσαρμοστεί για να παράγει περισσότερο αιθέρα.
Η αφυδάτωση της φάσης ατμού αιθανόλης παρουσία καταλυτών αλουμίνας, μπορεί να δώσει απόδοση 95% στην παραγωγή αιθυλαιθέρα.
Τοξικότητα
Μπορεί να προκαλέσει ερεθισμό στο δέρμα και στα μάτια με επαφή. Η επαφή με το δέρμα μπορεί να προκαλέσει το στέγνωμα και τη διάσπασή του. Ο αιθέρας συνήθως δεν διεισδύει στο δέρμα, καθώς εξατμίζεται γρήγορα.
Ο ερεθισμός των οφθαλμών που προκαλείται από τον αιθέρα είναι συνήθως ήπιος και σε περίπτωση σοβαρού ερεθισμού η βλάβη είναι συνήθως αναστρέψιμη.
Η κατάποσή του προκαλεί ναρκωτικές επιδράσεις και ερεθισμό του στομάχου. Η σοβαρή κατάποση μπορεί να προκαλέσει νεφρική βλάβη.
Η εισπνοή του αιθέρα μπορεί να προκαλέσει ερεθισμό της μύτης και του λαιμού. Σε περίπτωση εισπνοής αιθέρα μπορεί να συμβεί: υπνηλία, ενθουσιασμός, ζάλη, έμετος, ακανόνιστη αναπνοή και αυξημένη σιαλγία.
Η υψηλή έκθεση μπορεί να προκαλέσει απώλεια συνείδησης και ακόμη και θάνατο.
Η OSHA καθορίζει ένα όριο επαγγελματικής έκθεσης 800 ppm κατά μέσο όρο κατά τη διάρκεια μιας 8ωρης μετατόπισης.
Επίπεδα ερεθισμού των οφθαλμών: 100 ppm (άνθρωπος). Επίπεδα ερεθισμού των οφθαλμών: 1200 mg / m3 (400 ppm).
Χρησιμοποιεί
Οργανικός διαλύτης
Είναι ένας οργανικός διαλύτης που χρησιμοποιείται για τη διάλυση βρωμίου, ιωδίου και άλλων αλογόνων. η πλειοψηφία των λιπιδίων (λίπη), ρητίνες, καθαρά ελαστικά, μερικά αλκαλοειδή, κόμμεα, αρώματα, οξική κυτταρίνη, νιτρική κυτταρίνη, υδρογονάνθρακες και χρωστικές.
Επιπλέον, χρησιμοποιείται στην εκχύλιση των ενεργών συστατικών των ζωικών ιστών και φυτών, επειδή έχει μικρότερη πυκνότητα από το νερό και επιπλέει επ 'αυτού, αφήνοντας τις επιθυμητές ουσίες διαλυμένες στον αιθέρα.
Γενική αναισθησία
Έχει χρησιμοποιηθεί ως γενικό αναισθητικό από το 1840, αντικαθιστώντας το χλωροφόρμιο ως θεραπευτικό πλεονέκτημα. Ωστόσο, είναι μια εύφλεκτη ουσία και επομένως αντιμετωπίζει σοβαρές δυσκολίες για τη χρήση της μέσα σε κλινικές συνθήκες.
Επιπλέον, παράγει σε ασθενείς μερικές ανεπιθύμητες μετεγχειρητικές παρενέργειες όπως ναυτία και έμετο.
Για τους λόγους αυτούς, η χρήση του αιθέρα ως γενικού αναισθητικού έχει απορριφθεί, αντικαθιστώντας τον με άλλα αναισθητικά όπως το αλοθάνιο..
Πνεύμα του αιθέρα
Ο αιθέρας που αναμείχθηκε με αιθανόλη χρησιμοποιήθηκε για να σχηματίσει το διάλυμα που ονομάζεται πνεύμα αιθέρα, που χρησιμοποιείται στη θεραπεία της γαστρικής μετεωρίωσης και των ηπιότερων μορφών γαστραλγίας.
Αξιολόγηση της κυκλοφορίας του αίματος
Ο αιθέρας έχει χρησιμοποιηθεί για την αξιολόγηση της κυκλοφορίας του αίματος μεταξύ του βραχίονα και των πνευμόνων. Ο αιθέρας εγχέεται σε ένα βραχίονα, φέρνοντας το αίμα στο δεξιό κόλπο, κατόπιν στη δεξιά κοιλία και από εκεί στους πνεύμονες.
Ο χρόνος από την έγχυση του αιθέρα, μέχρι την αιθέρα πρόσληψη οσμή στον εκπνεόμενο αέρα, είναι περίπου 4 έως 6 s.
Διδακτικά εργαστήρια
Ο αιθέρας χρησιμοποιείται σε εργαστήρια διδασκαλίας σε πολλά πειράματα. για παράδειγμα, στην επίδειξη των νόμων της γενετικής του Mendel.
Ο αιθέρας χρησιμοποιείται για να αμβλύνει τις μύγες του γένους Drosophila και να επιτρέψει τις αναγκαίες διασταυρώσεις μεταξύ τους, προκειμένου να τεκμηριώσει τους νόμους της γενετικής
Αναφορές
- Graham Solomons T.W., Craig Β. Fryhle. (2011). Οργανική Χημεία. Αμίνες (10th έκδοση.). Wiley Plus.
- Carey F. (2008). Οργανική Χημεία (Έκτη έκδοση). Mc Graw Hill.
- Ο Σέβιερ. (2018). Διαιθυλαιθέρας. Science Direct. Ανακτήθηκε από: sciencedirect.com
- Οι συντάκτες της Εγκυκλοπαίδειας Britannica. (2018). Αιθυλαιθέρας. Britannica ncyclopædia. Ανακτήθηκε από: britannica.com
- PubChem (2018). Αιθέρας. Ανακτήθηκε από: pubchem.ncbi.nlm.nih.gov
- Wikipedia. (2018). Διαιθυλαιθέρας. Ανακτήθηκε από: en.wikipedia.org
- Φύλλο ασφάλειας XI: αιθυλαιθέρας. [PDF] Ανάκτηση από: quimica.unam.mx


