Ιδιότητες υδριδίου νατρίου (NaH), αντιδραστικότητα, κίνδυνοι και χρήσεις
Το υδρίδιο του νατρίου είναι μια ανόργανη ένωση του τύπου NaH. Έχει ιονικό δεσμό μεταξύ νατρίου και υδριδίου. Η δομή του απεικονίζεται στο Σχήμα 1 είναι αντιπροσωπευτική της αλατούχου υδρίδια, που σημαίνει ότι είναι παρόμοιο με υδρίδιο άλας, το οποίο περιλαμβάνει ιόντα Na + και Η, σε αντίθεση με τα μοριακά υδρίδια όπως το βοράνιο, το μεθάνιο, αμμωνία και νερό.
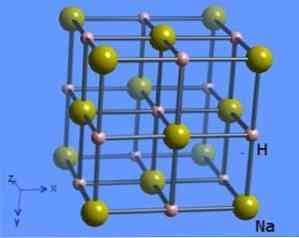
Η κρυσταλλική δομή έχει ένα αριθμό συνεργίας 6, όπου κάθε μόριο περιβάλλεται από ιόντα υδριδίου του νατρίου 8 παρουσιάζοντας μια οκταεδρική μορφή και απεικονίζεται στο Σχήμα 2 (Mark Winter [Το Πανεπιστήμιο του Sheffield Ltd και WebElements, 1993-2016).
Η ένωση παρασκευάζεται με την άμεση αντίδραση μεταξύ νατρίου και αέριο υδρογόνο (Νάτριο υδρίδιο Τύπου - Νάτριο Χρήσεις υδρίδιο, Properties, Δομή και του Τύπου, 2005-2017) ως εξής:
H2 + 2Na → 2NaH
Υδρίδιο του νατρίου πωλείται στο εμπόριο ως μια μορφή διασποράς 60% w / w (βάρος κατά ποσοστό βάρους) εντός ορυκτελαίου για ασφαλή χειρισμό (υδρίδιο του νατρίου, N.D.).
Ευρετήριο
- 1 Φυσικές και χημικές ιδιότητες του υδριδίου του νατρίου
- 2 Δραστικότητα και κίνδυνοι
- 3 Χρήσεις
- 4 Αναφορές
Φυσικές και χημικές ιδιότητες του υδριδίου του νατρίου
Το υδρίδιο του νατρίου είναι ένα λευκό στερεό όταν είναι καθαρό αν και γενικά αποκτάται σε γκρι ή σε ασήμι. Η εμφάνισή του φαίνεται στο σχήμα 3.

Το NaH έχει μοριακό βάρος 23,99771 g / mol, πυκνότητα 1,396 g / ml και σημείο τήξης 800 ° C (Royal Society of Chemistry, 2015). Είναι αδιάλυτο σε αμμωνία, βενζόλιο, τετραχλωράνθρακα και διθειάνθρακα (National Center for Biotechnology Information, s.f.).
Η ένωση είναι εξαιρετικά ασταθής. Το καθαρό NaH μπορεί εύκολα να αναφλεγεί στον αέρα. Όταν έρχεται σε επαφή με το νερό που υπάρχει στον αέρα, απελευθερώνει πολύ εύφλεκτο υδρογόνο.
Όταν είναι ανοικτό στον αέρα και στην υγρασία, το NaH υδρολύεται επίσης εύκολα στην ισχυρή διαβρωτική βάση υδροξειδίου του νατρίου (NaOH) σύμφωνα με την αντίδραση:
NaH + Η2Ο → ΝαΟΗ + Η2
Σε αυτή την αντίδραση μπορεί να παρατηρηθεί ότι το υδρίδιο του νατρίου συμπεριφέρεται σαν βάση. Αυτό οφείλεται στην ηλεκτροαρνησία.
Νάτριο έχει μια σημαντικά χαμηλότερη ηλεκτραρνητικότητα (≈1,0) εκτός από υδρογόνο (≈2,1), πράγμα που σημαίνει ότι το υδρογόνο εκχυλίζεται πυκνότητα ηλεκτρονίων προς τον εαυτό της και μακριά από το νάτριο για να παραχθεί ένα κατιόν νατρίου και ανιόν του υδριδίου.
Για μία ένωση να υπάρχει ανάγκη οξύ Bronsted να διαχωρίσει την ηλεκτρονιακή πυκνότητα του υδρογόνου, δηλαδή συνδέεται με ένα ηλεκτροαρνητικό άτομο όπως οξυγόνο, φθόριο, άζωτο, κλπ Μόνο τότε, μπορεί τυπικά να περιγραφεί ως Η + και μπορεί να διαχωριστεί ως τέτοιο.
Ένα υδρίδιο περιγράφεται πολύ καλύτερα ως Η- και έχει ένα ελεύθερο ζεύγος ηλεκτρονίων. Ως εκ τούτου, είναι μια βάση Brønsted, όχι ένα οξύ. Στην πραγματικότητα, εάν επεκτείνετε τον ορισμό οξέος / βάσης Brønsted με τον τρόπο που έκανε ο Lewis, θα καταλήξετε στο συμπέρασμα ότι το νάτριο (Na +) είναι το όξινο είδος εδώ.
Το προϊόν αντίδρασης Brønsted οξέος / βάσης της βάσης Η και του Η + οξέος γίνεται Η2. Επειδή το όξινο υδρογόνο εκχυλίζεται απ 'ευθείας από το νερό, το αέριο υδρογόνο μπορεί να φυσαλίδων, μετατοπίζοντας την ισορροπία ακόμη και αν η αντίδραση δεν ευνοείται θερμοδυναμικά.
Μπορούν να είναι ιόντα ΟΗ- που μπορεί να γραφτεί με την υπόλοιπη Na + κατιόντος για να δώσει υδροξείδιο του νατρίου (στερεό υδρίδιο νατρίου Γιατί βασίζεται και όχι ένα οξύ όταν αντιδράσει με νερό;, 2016).
Δραστικότητα και κίνδυνοι
Η ένωση είναι ένας ισχυρός αναγωγικός παράγοντας. Επιθέσεις SiO2 σε γυαλί. Είναι αναφλέγεται κατά την επαφή με το F2, Cl2, Br2 και αερίου I2 (το τελευταίο σε θερμοκρασίες άνω των 100 ° C), ειδικά με την παρουσία της υγρασίας για να σχηματιστεί HF, HCl, HBr και ΗΙ.
Αντιδρά με θείο για να δώσει Na2S και H2S. Μπορεί να αντιδρά εκρηκτικά με διμεθυλοσουλφοξείδιο. Αντιδρά έντονα με ακετυλένιο, ακόμη και στους -60 ° C. Είναι αυθόρμητα εύφλεκτο σε φθόριο.
Ξεκινά μια αντίδραση πολυμερισμού σε 2,2,3-τριφθοροπροπιονικό αιθυλεστέρα, έτσι ώστε ο εστέρας αποσυντίθεται βίαια. Η παρουσία στην αντίδραση ηλεκτρικού διαιθυλεστέρα και τριφθοροξικού αιθυλεστέρα, προκάλεσε εκρήξεις (HYDRIDE SODIUM, 2016).
Το υδρίδιο του νατρίου θεωρείται διαβρωτικό για το δέρμα ή τα μάτια, λόγω του δυναμικού των καυστικών υποπροϊόντων αντιδράσεων με το νερό.
Σε περίπτωση επαφής με τα μάτια, πρέπει να ξεπλυθούν με μεγάλες ποσότητες νερού, κάτω από τα βλέφαρα για τουλάχιστον 15 λεπτά και να αναζητήσουν αμέσως ιατρική βοήθεια..
Σε περίπτωση επαφής με το δέρμα, βουρτσίστε αμέσως και ξεπλύνετε την πληγείσα περιοχή με νερό. Ζητήστε ιατρική φροντίδα εάν ο ερεθισμός παραμένει.
Είναι επιβλαβές από την κατάποση λόγω της αντίδρασης στο νερό. Μην προκαλείτε εμετό. Θα πρέπει να αναζητήσετε αμέσως ιατρική βοήθεια και να μεταφέρετε το θύμα σε ιατρικό κέντρο.
Η διασπορά του υδριδίου του νατρίου στο πετρέλαιο δεν είναι σκόνη. Ωστόσο, το υλικό που αντιδρά μπορεί να εκπέμψει μια λεπτή καυστική ομίχλη. Σε περίπτωση εισπνοής, ξεπλύνετε το στόμα με νερό και μεταφέρετε το θύμα σε ένα μέρος με καθαρό αέρα. Πρέπει να αναζητηθεί ιατρική φροντίδα (Rhom and Hass Inc., 2007).
Χρησιμοποιεί
Η κύρια χρήση του υδριδίου του νατρίου είναι η πραγματοποίηση αντιδράσεων συμπύκνωσης και αλκυλίωσης που αναπτύσσονται μέσω του σχηματισμού ενός καρβανιόντος (καταλυόμενου από τη βάση).
υδριδίου του νατρίου σε έλαιο μοιάζει αλκοολικά νάτριο και μεταλλικό νάτριο στην ικανότητά της να λειτουργεί ως ένας παράγοντας αποπρωτονίωσης σε ακετοξικού εστέρα, συμπυκνώσεις Claisen, Stobbe, Dieckmann και συναφείς αντιδράσεις. Έχει αξιοσημείωτα πλεονεκτήματα έναντι άλλων παραγόντων συμπύκνωσης στο ότι:
- Είναι μια ισχυρότερη βάση, η οποία οδηγεί σε μια πιο άμεση αποπρωτονίωση.
- Δεν απαιτείται υπέρβαση.
- Το παραγόμενο Η2 δίνει ένα μέτρο της έκτασης της αντίδρασης.
- Οι δευτερογενείς αντιδράσεις όπως οι μειώσεις εξαλείφονται.
Αλκυλώσεις αρωματικών και ετεροκυκλικών αμινών όπως η 2-αμινοπυριδίνη και η φαινοθειαζίνη επιτυγχάνονται εύκολα με υψηλή απόδοση χρησιμοποιώντας μίγματα τολουολίου-μεθυλοφορμαμιδίου. Η συγκέντρωση του διμεθυλοφορμαμιδίου είναι μια μεταβλητή που χρησιμοποιείται για τον έλεγχο του ρυθμού αντίδρασης (HINCKLEY, 1957).
Έχει προταθεί η χρήση υδριδίου του νατρίου για την αποθήκευση υδρογόνου για χρήση σε οχήματα κυψελών καυσίμου, το υδρίδιο του υδρογόνου να χωρέσει σε πλαστική κοκκία κονιοποιημένο υπό την παρουσία νερού για να απελευθερώσει.
Αναφορές
- HINCKLEY, Μ. D. (1957). Κατασκευή, χειρισμός και χρήση υδριδίου του νατρίου. Advances in Chemistry, Τόμος 19, 106-117.
- Mark Winter [Το Πανεπιστήμιο του Sheffield και WebElements Ltd, U. (1993-2016). Νάτριο: υδρίδιο του νατρίου. Ανακτήθηκε από το WebElements: webelements.com.
- Εθνικό Κέντρο Βιοτεχνολογικών Πληροφοριών. (s.f.). Δημοσιευμένη βάση δεδομένων PubChem. CID = 24758. Ανακτήθηκε από το PubChem: pubchem.ncbi.nlm.nih.gov.
- Rhom και Hass inc. (2007, Δεκέμβριος). Υδρίδιο του νατρίου 60% διασπορά σε λάδι. Ανακτήθηκε από το dow.com.
- Βασιλική Εταιρεία Χημείας. (2015). Υδρίδιο του νατρίου. Ανακτήθηκε από το ChemSpider: chemspider.com.
- ΥΔΡΟΫΔΙΟ ΝΑΤΡΙΟΥ. (2016). Ανακτήθηκε από αιματοχημικά: cameochemicals.noaa.gov.
- Υδρίδιο του νατρίου Τύπος - Υδρίδιο του νατρίου Χρήσεις, ιδιότητες, δομή και τύπος. (2005-2017). Ανακτήθηκε από το Softschools.com: softschools.com.
- ΥΔΡΟΫΔΙΟ ΝΑΤΡΙΟΥ. (s.f.). Ανακτήθηκε από chemicalland21: chemicalland21.com.
- Γιατί είναι το στερεό υδρίδιο του νατρίου και όχι το οξύ όταν αντιδρά με νερό; (2016, 20 Απριλίου). Ανακτήθηκε από stackexchange: chemistry.stackexchange.com.


