Δομή υδροβρωμικού οξέος (HBr), ιδιότητες, σχηματισμός, χρήσεις
Το Υδροβρωμικό οξύ είναι μια ανόργανη ένωση που προκύπτει από το υδατικό διάλυμα ενός αερίου που ονομάζεται υδροβρώμιο. Ο χημικός τύπος του είναι HBr και μπορεί να θεωρηθεί με διαφορετικούς τρόπους ισοδύναμο: ως μοριακό υδρίδιο ή αλογονίδιο υδρογόνου στο νερό. δηλαδή, ένα υδραζίδιο.
Στις χημικές εξισώσεις, πρέπει να γράφεται ως HBr (ac), για να δείξει ότι είναι υδροβρωμικό οξύ και όχι αέριο. Αυτό το οξύ είναι ένα από τα ισχυρότερα γνωστά, ακόμη περισσότερο από υδροχλωρικό οξύ, HCl. Η εξήγηση γι 'αυτό έγκειται στη φύση του ομοιοπολικού δεσμού του.
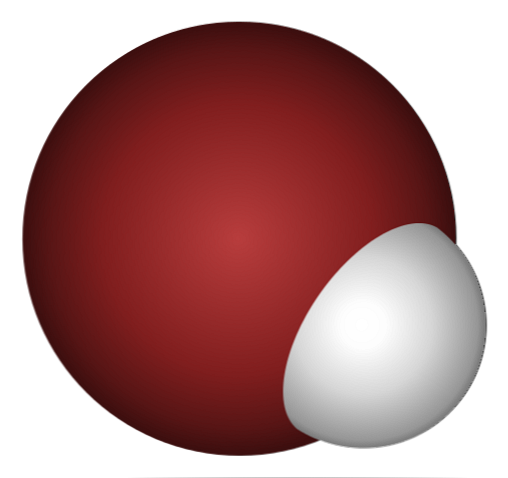
Γιατί το HBr είναι ένα τέτοιο οξύ και ακόμα πιο διαλυμένο στο νερό; Επειδή ο ομοιοπολικός δεσμός H-Br είναι πολύ αδύναμη λόγω της κακής επικάλυψη των 1s τροχιακό από Η και Br 4p.
Αυτό δεν προκαλεί έκπληξη αν κοιτάξετε προσεκτικά την εικόνα παραπάνω, όπου σαφώς το άτομο βρωμίου (καφέ) είναι πολύ μεγαλύτερο από το άτομο υδρογόνου (λευκό).
Κατά συνέπεια, οποιαδήποτε διαταραχή προκαλεί την διάσπαση του δεσμού Η-Βγ, απελευθερώνοντας το ιόν Η+. Στη συνέχεια, το υδροβρωμικό οξύ είναι ένα οξύ Brönsted, δεδομένου ότι μεταφέρει πρωτόνια ή ιόντα υδρογόνου. Η αντοχή του είναι τέτοια που χρησιμοποιείται στη σύνθεση διαφόρων οργανοβρωμιωμένων ενώσεων (όπως 1-βρωμοαιθάνιο, CH3CH2Br).
Υδροβρωμικό οξύ είναι, μετά yohídrico, ΗΙ, ένα από τα ισχυρότερα και υδραζίδια χρήσιμα για την πέψη των ορισμένων στερεών δειγμάτων.
Ευρετήριο
- 1 Δομή του υδροβρωμικού οξέος
- 1.1 Οξύτητα
- 2 Φυσικές και χημικές ιδιότητες
- 2.1 Μοριακός τύπος
- 2.2 Μοριακό βάρος
- 2.3 Φυσική εμφάνιση
- 2.4 Οσμή
- 2.5 Όριο οσμής
- 2.6 Πυκνότητα
- 2.7 Σημείο τήξης
- 2.8 Σημείο ζέσεως
- 2.9 Διαλυτότητα στο νερό
- 2.10 Πυκνότητα ατμών
- 2.11 pKa οξύτητα
- 2.12 Θερμική ικανότητα
- 2.13 Τυπική μοριακή ενθαλπία
- 2.14 Πρότυπη μοριακή εντροπία
- 2.15 Σημείο ανάφλεξης
- 3 Ονοματολογία
- 4 Πώς σχηματίζεται?
- 4.1 Μείγμα υδρογόνου και βρωμίου σε νερό
- 4.2 Τριβρωμιούχο φωσφόρο
- 4.3 Διοξείδιο του θείου και βρώμιο
- 5 Χρήσεις
- 5.1 Παρασκευή βρωμιδίων
- 5.2 Σύνθεση αλκυλαλογονιδίων
- 5.3 καταλύτης
- 6 Αναφορές
Δομή του υδροβρωμικού οξέος
Η δομή του Η-Βγ φαίνεται στην εικόνα, των οποίων οι ιδιότητες και τα χαρακτηριστικά, ακόμη και εκείνα του αερίου, είναι στενά συνδεδεμένα με τα υδατικά διαλύματα του. Γι 'αυτό έρχεται ένα σημείο όπου εισέρχεται σε μια σύγχυση ως προς το ποια από τις δύο ενώσεις αναφέρεται: HBr ή HBr (aq).
Η δομή του HBr (ac) είναι διαφορετική από αυτή του HBr, επειδή τώρα τα μόρια νερού διαλύουν αυτό το διατομικό μόριο. Όταν είναι αρκετά κοντά, το Η μεταφέρεται+ σε ένα μόριο Η2Ή όπως υποδεικνύεται στην ακόλουθη χημική εξίσωση:
HBr + Η2Ο => Br-- + H3Ο+
Έτσι, η δομή του υδροβρωμικού οξέος αποτελείται από ιόντα Βγ-- και Η3Ο+ αλληλεπιδρώντας ηλεκτροστατικά. Τώρα, είναι λίγο διαφορετικό από τον ομοιοπολικό δεσμό του H-Br.
Η μεγάλη οξύτητά του οφείλεται στο ογκώδες ανιόν Br- μπορεί μόλις να αλληλεπιδράσει με το Η3Ο+, δεν μπορεί να τον εμποδίσει να μεταφέρει το Η+ σε άλλο περιβάλλον χημικό είδος.
Οξύτητα
Για παράδειγμα, το Cl- και το F- αν και δεν σχηματίζουν ομοιοπολικούς δεσμούς με το Η3Ο+, μπορούν να αλληλεπιδρούν μέσω άλλων διαμοριακών δυνάμεων, όπως γέφυρες υδρογόνου (οι οποίες μόνο το F- είναι σε θέση να τα δεχτεί). Οι γέφυρες υδρογόνου F--Η-ΟΗ2+ "Παρεμπόδιση" της δωρεάς του Η+.
Γι 'αυτό το λόγο το υδροφθορικό οξύ, HF, είναι ασθενέστερο οξύ σε νερό από το υδροβρωμικό οξύ. δεδομένου ότι οι ιονικές αλληλεπιδράσεις Br- H3Ο+ μην ενοχλείστε τη μεταφορά του Η+.
Ωστόσο, αν και υπάρχει νερό στο HBr (ac), η συμπεριφορά του στο τέλος του λογαριασμού είναι παρόμοια με εκείνη ενός μορίου H-Br. δηλαδή, ένα Η+ Μεταφέρεται από HBr ή Br-H3Ο+.
Φυσικές και χημικές ιδιότητες
Μοριακός τύπος
HBr.
Μοριακό βάρος
80,972 g / mol. Σημειώστε ότι, όπως αναφέρεται στην προηγούμενη ενότητα, θεωρείται μόνο το HBr και όχι το μόριο του νερού. Εάν το μοριακό βάρος λαμβάνεται από τον τύπο Br-H3Ο+ θα έχει τιμή περίπου 99 g / mol περίπου.
Φυσική εμφάνιση
Άχρωμο ή ωχροκίτρινο υγρό, το οποίο εξαρτάται από τη συγκέντρωση διαλυμένου HBr. Όσο πιο κίτρινο είναι, τόσο πιο συγκεντρωμένο και επικίνδυνο θα είναι.
Οσμή
Οξεία, ενοχλητική.
Όριο οσμής
6,67 mg / m3.
Πυκνότητα
1,49 g / cm3 (υδατικό διάλυμα σε 48% β / β). Αυτή η τιμή, όπως αυτές που αντιστοιχούν στα σημεία τήξης και βρασμού, εξαρτάται από την ποσότητα του HBr που διαλύεται στο νερό.
Σημείο τήξης
-11 ° C (12 ° F, 393 ° Κ) (υδατικό διάλυμα σε 49% β / β).
Σημείο ζέσεως
122 ° C (252 ° F 393 ° Κ) σε 700 mmHg (υδατικό διάλυμα 47-49% β / β).
Διαλυτότητα στο νερό
-221 g / 100 ml (στους 0 ° C).
-204 g / 100 ml (15 ° C).
-130 g / 100 ml (100 ° C).
Αυτές οι τιμές αναφέρονται σε αέρια HBr, όχι σε υδροβρωμικό οξύ. Όπως μπορεί να φανεί, η αύξηση της θερμοκρασίας μειώνει τη διαλυτότητα του HBr. συμπεριφορά που είναι φυσική στα αέρια. Συνεπώς, εάν απαιτούνται διαλύματα συμπυκνωμένου HBr (ac), είναι καλύτερο να εργαστείτε μαζί τους σε χαμηλές θερμοκρασίες.
Εάν εργάζεται σε υψηλές θερμοκρασίες, το HBr θα διαφύγει με τη μορφή αεριωδών διατομικών μορίων, οπότε ο αντιδραστήρας πρέπει να σφραγισθεί για να αποφευχθεί η διαρροή.
Πυκνότητα ατμών
2.71 (σε σχέση με τον αέρα = 1).
Οξύτητα pKa
-9,0. Αυτή η σταθερά τόσο αρνητική είναι ενδεικτική της μεγάλης ισχύος της οξύτητας.
Θερμική ικανότητα
29,1 kJ / mol.
Τυπική μοριακή ενθαλπία
198,7 kJ / mol (298 Κ).
Τυπική μοριακή εντροπία
-36,3 kJ / mol.
Σημείο ανάφλεξης
Δεν είναι εύφλεκτο.
Ονοματολογία
Η ονομασία του «υδροβρωμικό οξύ» συνδυάζει δύο γεγονότα: την παρουσία ύδατος, και ότι το βρώμιο έχει σθένος -1 στην ένωση. Στην αγγλική γλώσσα είναι κάπως περισσότερο εμφανής: το υδροβρωμικό οξύ, όπου το πρόθεμα «υδρογόνο» (ή υδρογόνο) αναφέρεται στο νερό. αν και, στην πραγματικότητα, μπορεί επίσης να αναφέρεται στο υδρογόνο.
Το βρώμιο έχει σθένος -1 επειδή δεσμεύεται από το άτομο υδρογόνου λιγότερο ηλεκτροαρνητικό από ό, τι είναι. αλλά εάν συνδέεται ή αλληλεπιδρά με άτομα οξυγόνου, μπορεί να έχει πολλά σθένη, όπως: +2, +3, +5 και +7. Με το Η μπορεί να υιοθετήσει μόνο ένα σθένος, και αυτός είναι ο λόγος που το suffix -ico προστίθεται στο όνομά του.
Ενώ το HBr (g), υδροβρώμιο, είναι άνυδρο. δηλαδή, δεν έχει νερό. Ως εκ τούτου, ονομάζεται σύμφωνα με άλλα πρότυπα ονοματολογίας, που αντιστοιχούν σε εκείνα των αλογονιδίων υδρογόνου.
Πώς σχηματίζεται?
Υπάρχουν αρκετές συνθετικές μέθοδοι για την παρασκευή του υδροβρωμικού οξέος. Μερικά από αυτά είναι:
Μείγμα υδρογόνου και βρωμίου στο νερό
Χωρίς να περιγράφονται οι τεχνικές λεπτομέρειες, αυτό το οξύ μπορεί να ληφθεί από το άμεσο μίγμα υδρογόνου και βρωμίου σε έναν αντιδραστήρα γεμάτο με νερό.
H2 + Br2 => HBr
Με αυτόν τον τρόπο, καθώς οι μορφές HBr διαλύονται στο νερό, Αυτό μπορεί να το σύρετε στις αποστάξεις, έτσι ώστε τα διαλύματα να μπορούν να εξαχθούν με διαφορετικές συγκεντρώσεις. Το υδρογόνο είναι ένα αέριο και το βρώμιο ένα σκούρο κοκκινωπό υγρό.
Τριβρωμιούχο φωσφόρο
Σε μια πιο περίπλοκη διαδικασία, η άμμος, ο ενυδατωμένος κόκκινος φώσφορος και το βρώμιο αναμειγνύονται. Οι παγίδες νερού τοποθετούνται σε παγόλουτρα για να αποτραπεί η διαφυγή του HBr και το σχηματισμό του υδροβρωμικού οξέος. Οι αντιδράσεις είναι:
2P + 3Br2 => 2PBr3
PBr3 + 3Η2Ο => 3ΗΒγ + Η3PO3
Διοξείδιο του θείου και βρώμιο
Ένας άλλος τρόπος παρασκευής του είναι η αντίδραση του βρωμίου με διοξείδιο του θείου σε νερό:
Br2 + Έτσι2 + 2Η2Ο => 2HBr + Η2Έτσι4
Αυτή είναι μια αντίδραση οξειδοαναγωγής. Το Br2 μειώνει, κερδίζει ηλεκτρόνια, συνδέοντας με τα υδρογόνα. ενώ το SO2 οξειδώνει, χάνει ηλεκτρόνια, όταν σχηματίζει περισσότερους ομοιοπολικούς δεσμούς με άλλα οξυγόνα, όπως στο θειικό οξύ.
Χρησιμοποιεί
Παρασκευή βρωμιδίων
Τα άλατα βρωμιδίου μπορούν να παρασκευασθούν αν η HBr (ac) αντιδρά με ένα υδροξείδιο μετάλλου. Για παράδειγμα, εξετάζεται η παραγωγή βρωμιούχου ασβεστίου:
Ca (ΟΗ)2 + 2HBr => CaBr2 + H2Ο
Ένα άλλο παράδειγμα είναι το βρωμιούχο νάτριο:
NaOH + HBr => NaBr + Η2Ο
Έτσι, πολλά από τα ανόργανα βρωμίδια μπορούν να παρασκευαστούν.
Σύνθεση αλκυλαλογονιδίων
Και τι γίνεται με τα οργανικά βρωμίδια; Αυτές είναι οργανοβρωμιωμένες ενώσεις: RBr ή ArBr.
Αφυδάτωση αλκοολών
Η πρώτη ύλη για την απόκτηση τους μπορεί να είναι οι αλκοόλες. Όταν πρωτονιοποιούνται από την οξύτητα του HBr, σχηματίζουν νερό, το οποίο είναι μια καλή εξερχόμενη ομάδα και αντ 'αυτού ενσωματώνεται το ογκώδες άτομο του Br που θα συνδέεται ομοιοπολικά με τον άνθρακα:
ROH + HBr => RBr + Η2Ο
Αυτή η αφυδάτωση πραγματοποιείται σε θερμοκρασίες άνω των 100 ° C, προκειμένου να διευκολυνθεί η ρήξη του δεσμού R-OH2+.
Προσθήκη σε αλκένια και αλκύνια
Το μόριο HBr μπορεί να προστεθεί από το υδατικό του διάλυμα στον διπλό ή τριπλό δεσμό ενός αλκενίου ή αλκινίου:
R2C = CR2 + HBr => RHC-CRBr
RC = CR + HBr => RHC = CRBr
Μπορούν να ληφθούν διάφορα προϊόντα, αλλά υπό απλές συνθήκες, το προϊόν σχηματίζεται αρχικά όπου το βρώμιο συνδέεται με δευτεροταγή, τριτοταγή ή τεταρτοταγή άνθρακα (κανόνας Markovnikov).
Αυτά τα αλογονίδια παρεμβαίνουν στη σύνθεση άλλων οργανικών ενώσεων και το εύρος των χρήσεών τους είναι πολύ εκτεταμένο. Επίσης, μερικές από αυτές μπορούν ακόμη να χρησιμοποιηθούν στη σύνθεση ή το σχεδιασμό νέων φαρμάκων.
Αιθερική διάσπαση
Από τους αιθέρες, δύο αλκυλαλογονίδια μπορούν να ληφθούν ταυτοχρόνως, καθένα από τα οποία φέρει μία από τις δύο πλευρικές αλυσίδες R ή R 'του αρχικού αιθέρα R-O-R'. Συμβαίνει κάτι παρόμοιο με την αφυδάτωση των αλκοολών, αλλά ο μηχανισμός αντίδρασης είναι διαφορετικός.
Η αντίδραση μπορεί να σχηματοποιηθεί με την ακόλουθη χημική εξίσωση:
ROR '+ 2HBr => RBr + R'Br
Και το νερό απελευθερώνεται επίσης.
Καταλύτης
Η οξύτητά του είναι τέτοια ώστε να μπορεί να χρησιμοποιηθεί ως αποτελεσματικός καταλύτης οξέος. Αντί να προστεθεί το ανιόν Br- με τη μοριακή δομή, ανοίγει το δρόμο για ένα άλλο μόριο για να το κάνει.
Αναφορές
- Graham Solomons T.W., Craig Β. Fryhle. (2011). Οργανική Χημεία. Αμίνες (10th έκδοση.). Wiley Plus.
- Carey F. (2008). Οργανική Χημεία (Έκτη έκδοση). Mc Graw Hill.
- Steven A. Hardinger. (2017). Εικονογραφημένο Γλωσσάρι Οργανικής Χημείας: Υδροβρωμικό οξύ. Ανακτήθηκε από: chem.ucla.edu
- Wikipedia. (2018). Υδροβρωμικό οξύ. Ανακτήθηκε από: en.wikipedia.org
- PubChem. (2018). Υδροβρωμικό οξύ. Ανακτήθηκε από: pubchem.ncbi.nlm.nih.gov
- Εθνικό Ινστιτούτο για την Ασφάλεια και την Υγιεινή στην Εργασία. (2011). Βρωμιούχο υδρογόνο [PDF] Ανακτήθηκε από: insht.es
- PrepChem. (2016). Παρασκευή υδροβρωμικού οξέος. Ανακτήθηκε από: prepchem.com


