Κυκλοεξενική δομή, ιδιότητες, σύνθεση και χρήσεις
Το κυκλοεξένιο είναι ένα αλκένιο ή κυκλική ολεφίνη του οποίου ο μοριακός τύπος είναι C6H10. Αποτελείται από ένα άχρωμο υγρό, αδιάλυτο στο νερό και αναμίξιμο με πολλούς οργανικούς διαλύτες. Χαρακτηρίζεται από το ότι είναι εύφλεκτο, και στη φύση του συνήθως απαντάται σε λιθανθρακόπισσα..
Το κυκλοεξάνιο συντίθεται με μερική υδρογόνωση του βενζολίου και με αφυδάτωση της αλκοόλης κυκλοεξανόλης. δηλαδή, μια πιο σκουριασμένη μορφή. Όπως και άλλα κυκλοαλκένια, υφίσταται αντιδράσεις ηλεκτροφιλικής προσθήκης και με ελεύθερες ρίζες. για παράδειγμα, την αντίδραση αλογόνωσης.

Αυτή η κυκλική αλκένιο (κορυφή) μορφή (μη διαχωριζόμενες, με απόσταξη) αζεοτροπικά μίγματα με κατώτερες αλκοόλες και οξικό οξύ. Δεν είναι πολύ σταθερό σε παρατεταμένη αποθήκευση, καθώς αποσυντίθεται κάτω από τη δράση του ηλιακού φωτός και της υπεριώδους ακτινοβολίας.
Το κυκλοεξένιο χρησιμοποιείται ως διαλύτης, και ως εκ τούτου έχει πολλές εφαρμογές, όπως σταθεροποιητή της βενζίνης υψηλού αριθμού οκτανίου και για την εκχύλιση ελαίων.
Αλλά το πιο σημαντικό, είναι ότι το κυκλοεξένιο είναι ο ενδιάμεσος και πρώτης ύλης για την παρασκευή πολυάριθμων ενώσεων χρήσιμων, συμπεριλαμβανομένων: κυκλοεξανόνη, αδιπικό οξύ, μηλεϊνικό οξύ, κυκλοεξάνιο, βουταδιένιο, κυκλοεξυλκαρβοξυλικού οξύ, κλπ.
Ευρετήριο
- 1 Δομή κυκλοεξενίου
- 1.1 Διαμοριακές αλληλεπιδράσεις
- 2 Ιδιότητες
- 2.1 Χημικές ονομασίες
- 2.2 Μοριακό βάρος
- 2.3 Φυσική εμφάνιση
- 2.4 Οσμή
- 2.5 Σημείο ζέσης
- 2.6 Σημείο τήξης
- 2.7 Σημείο ανάφλεξης
- 2.8 Διαλυτότητα στο νερό
- 2.9 Διαλυτότητα σε οργανικούς διαλύτες
- 2.10 Πυκνότητα
- 2.11 Πυκνότητα ατμών
- 2.12 Πίεση ατμών
- 2.13 Αυτο-ανάφλεξη
- 2.14 Αποσύνθεση
- 2.15 Ιξώδες
- 2.16 Θερμότητα καύσης
- 2.17 Θερμοκρασία εξάτμισης
- 2.18 Επιφανειακή τάση
- 2.19 Πολυμερισμός
- 2.20 Όριο οσμής
- 2.21 Δείκτης διαθλάσεως
- 2,22 ρΗ
- 2.23 Σταθερότητα
- 2.24 Αντιδράσεις
- 3 Περίληψη
- 4 Χρήσεις
- 5 Κίνδυνοι
- 6 Αναφορές
Δομή κυκλοεξενίου
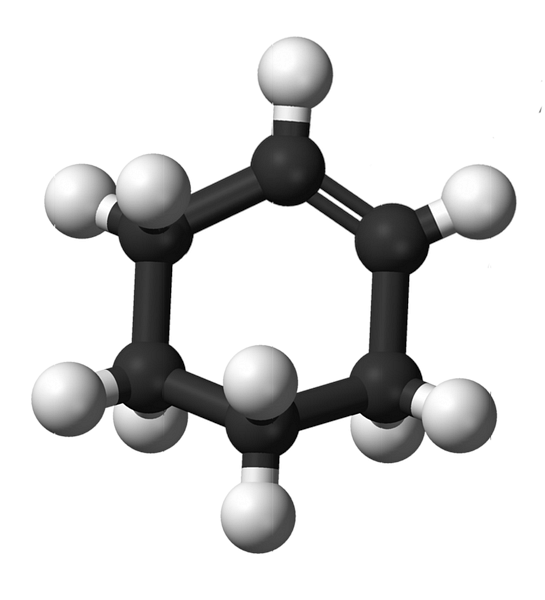
Η δομή του κυκλοεξενίου με ένα μοντέλο σφαιρών και ράβδων παρουσιάζεται στην παραπάνω εικόνα. Μπορεί να παρατηρηθεί ο δακτύλιος άνθρακα των έξι ατόμων και ο διπλός δεσμός, και οι δύο ακορεστότητες της ένωσης. Από αυτή την άποψη, φαίνεται ότι ο δακτύλιος είναι επίπεδος. αλλά δεν είναι καθόλου.
Για αρχάριους, οι άνθρακες του διπλού δεσμού έχουν sp υβριδισμό2, που τους δίνει τριγωνική γεωμετρία. Επομένως, αυτοί οι δύο άνθρακες, και αυτοί που τους γειτονεύουν, βρίσκονται στο ίδιο επίπεδο. ενώ οι δύο άνθρακες στο αντίθετο άκρο (στον διπλό δεσμό) είναι πάνω και κάτω από το εν λόγω επίπεδο.
Η κάτω εικόνα απεικονίζει απόλυτα αυτό που έχει μόλις εξηγηθεί.

Σημειώστε ότι η μαύρη ζώνη αποτελείται από τέσσερις άνθρακες: τους δύο από τους διπλούς δεσμούς, και τους άλλους δίπλα τους. Η εκτεθειμένη προοπτική είναι αυτή που θα μπορούσε να επιτευχθεί εάν ένας θεατής έβαλε το μάτι του ακριβώς μπροστά από τον διπλό δεσμό. Μπορεί να δει κανείς ότι ένας άνθρακας είναι πάνω και κάτω από αυτό το επίπεδο.
Δεδομένου ότι το μόριο του κυκλοεξενίου δεν είναι στατικό, οι δύο άνθρακες θα αλλάξουν: το ένα θα μειωθεί ενώ το άλλο θα ανέβει πάνω από το επίπεδο. Έτσι θα περίμενε κανείς ότι το μόριο θα συμπεριφερθεί.
Διαμοριακές αλληλεπιδράσεις
Το κυκλοεξένιο είναι ένας υδρογονάνθρακας και συνεπώς οι διαμοριακές αλληλεπιδράσεις του βασίζονται στις δυνάμεις διασποράς του Λονδίνου.
Αυτό οφείλεται στο γεγονός ότι το μόριο είναι απολιτικό, χωρίς μόνιμη διπολική ροπή, και το μοριακό του βάρος είναι ο παράγοντας που συμβάλλει περισσότερο στη διατήρηση της συνεκτικότητας του στο υγρό.
Επίσης, ο διπλός δεσμός αυξάνει το βαθμό της αλληλεπίδρασης, καθώς δεν μπορεί να κινηθεί με την ίδια ευελιξία ως το άλλο άνθρακα, και αυτό προάγει την αλληλεπίδραση μεταξύ γειτονικών μορίων. Είναι για αυτόν τον λόγο ότι η κυκλοεξένιο έχει σημείο ζέσεως ελαφρώς υψηλότερη (83 ° C) απ 'ότι κυκλοεξανίου (81 ° C).
Ιδιότητες
Χημικές ονομασίες
Κυκλοεξένιο, τετραϋδροβενζόλιο.
Μοριακό βάρος
82,146 g / mol.
Φυσική εμφάνιση
Άχρωμο υγρό.
Οσμή
Γλυκιά μυρωδιά.
Σημείο ζέσεως
83 ºC έως 760 mmHg.
Σημείο τήξης
-103,5 ° C.
Σημείο ανάφλεξης
-7ºC (κλειστό δοχείο).
Διαλυτότητα στο νερό
Σχεδόν αδιάλυτο (213 mg / L).
Διαλυτότητα σε οργανικούς διαλύτες
Αναμείξιμο με αιθανόλη, βενζόλιο, τετραχλωράνθρακα, πετρελαϊκό αιθέρα και ακετόνη. Αναμένεται ότι θα είναι σε θέση να διαλύσει τις απολιθικές ενώσεις, όπως μερικά από τα αλλοτρόπια του άνθρακα.
Πυκνότητα
0,810 g / cm3 στους 20ºC.
Πυκνότητα ατμών
2.8 (σε σχέση με τον αέρα που λαμβάνεται ως ίσο με 1).
Πίεση ατμού
89 mmHg στους 25 ° C.
Αυτόματη ανάφλεξη
244 ºC.
Αποσύνθεση
Αποικοδομείται παρουσία αλάτων ουρανίου, υπό την επίδραση του ηλιακού φωτός και της υπεριώδους ακτινοβολίας.
Ιξώδες
0,625 mPascal στους 25 ° C.
Θερμότητα καύσης
3.751 kJ / mol στους 25 ° C.
Θερμοκρασία εξάτμισης
30,46 kJ / mol στους 25 ° C.
Επιφανειακή τάση
26,26 mN / m.
Πολυμερισμός
Μπορεί να πολυμεριστεί υπό ορισμένες συνθήκες.
Όριο οσμής
0,6 mg / m3.
Δείκτης διάθλασης
1,4465 στους 20 ºC.
ρΗ
7-8 στους 20ºC.
Σταθερότητα
Το κυκλοεξένιο δεν είναι πολύ σταθερό κατά τη διάρκεια μακροχρόνιας αποθήκευσης. Η έκθεση στο φως και στον αέρα μπορεί να προκαλέσει την παραγωγή υπεροξειδίων. Ομοίως, είναι ασύμβατο με ισχυρούς οξειδωτικούς παράγοντες.
Αντιδράσεις
-Τα κυκλοαλκένια εμφανίζουν κυρίως αντιδράσεις προσθήκης, τόσο ηλεκτρονιόφιλες όσο και ελεύθερες ρίζες.
-Αντιδρά με βρώμιο για να σχηματίσει 1,2-διβρωμοκυκλοεξάνιο.
-Οξειδώνεται γρήγορα με την παρουσία υπερμαγγανικού καλίου (KMnO4).
-Είναι ικανό να παράγει ένα εποξείδιο (κυκλοεξανοξείδιο) παρουσία υπεροξυβενζοϊκού οξέος.
Σύνθεση
Το κυκλοεξάνιο παράγεται με όξινη κατάλυση κυκλοεξανόλης:

Το σύμβολο Δ αντιπροσωπεύει την θερμότητα που απαιτείται για την προώθηση της εξόδου της ομάδας ΟΗ όπως μόριο νερού σε όξινο μέσο (-ΟΗ2+).
Το κυκλοεξένιο παράγεται επίσης με μερική υδρογόνωση του βενζολίου. δηλαδή, δύο από τους διπλούς δεσμούς προσθέτουν ένα μόριο υδρογόνου:

Αν και η αντίδραση φαίνεται απλή, απαιτεί μεγάλες πιέσεις του Η2 και καταλύτες.
Χρησιμοποιεί
-Έχει χρησιμότητα ως οργανικό διαλύτη. Επιπλέον, πρόκειται για πρώτη ύλη για την παραγωγή αδιπικού οξέος, αδιπικής αλδεΰδης, μηλεϊνικού οξέος, κυκλοεξανίου και κυκλοεξυλοκαρβοξυλικού οξέος.
-Χρησιμοποιείται στην παραγωγή κυκλοεξανιοχλωριδίου, μιας ένωσης που χρησιμοποιείται ως ενδιάμεσος στην παρασκευή φαρμακευτικών προϊόντων και πρόσθετων από καουτσούκ..
-Το κυκλοεξένιο χρησιμοποιείται επίσης στη σύνθεση της κυκλοεξανόνης, πρώτης ύλης για την παραγωγή φαρμάκων, παρασιτοκτόνων, αρωμάτων και βαφών.
-Το κυκλοεξένιο εμπλέκεται στη σύνθεση της αμινοκυκλοεξανόλης, μιας ένωσης που χρησιμοποιείται ως επιφανειοδραστική ουσία και γαλακτωματοποιητής..
-Επιπλέον, το κυκλοεξένιο μπορεί να χρησιμοποιηθεί για την παρασκευή στο εργαστήριο βουταδιενίου. Η τελευταία ένωση χρησιμοποιείται στην κατασκευή συνθετικού καουτσούκ, στην κατασκευή ελαστικών αυτοκινήτων και χρησιμοποιείται επίσης στην κατασκευή ακρυλικών πλαστικών.
-Το κυκλοεξένιο είναι η πρώτη ύλη για τη σύνθεση της λυσίνης, της φαινόλης, της ρητίνης πολυκυκλοολεφίνης και των πρόσθετων από καουτσούκ.
-Χρησιμοποιείται ως σταθεροποιητής βενζινών υψηλού οκτανίου.
-Συμμετέχει στη σύνθεση αδιάβροχων επικαλύψεων, μεμβράνες ανθεκτικές στη ρωγμή και δεσμευτικές συνδετικές ουσίες για επιχρίσματα.
Κίνδυνοι
Το κυκλοεξένιο δεν είναι μια πολύ τοξική ένωση, αλλά μπορεί να προκαλέσει ερυθρότητα του δέρματος και των ματιών μέσω επαφής. Η εισπνοή του μπορεί να προκαλέσει βήχα και υπνηλία. Επιπλέον, η κατάποσή του μπορεί να προκαλέσει υπνηλία, δυσκολία στην αναπνοή και ναυτία.
Το κυκλοεξένιο απορροφάται ελάχιστα στο γαστρεντερικό σωλήνα, επομένως δεν αναμένονται σοβαρές συστηματικές επιδράσεις λόγω της κατάποσης. Η μεγαλύτερη επιπλοκή είναι η αναρρόφηση από το αναπνευστικό σύστημα, το οποίο μπορεί να προκαλέσει χημική πνευμονία.
Αναφορές
- Joseph F. Chiang και Simon Harvey Bauer. (1968). Μοριακή δομή κυκλοεξενίου. J. Am., Chem. Soc. 1969, 91, 8, 1898-1901.
- Karry Barnes. (2019). Κυκλοεξένιο: Κίνδυνοι, Σύνθεση & Δομή. Μελέτη. Ανακτήθηκε από: study.com
- Morrison, R. Τ. And Boyd, R. Ν. (1987). Οργανική Χημεία (5ta Έκδοση.). Συντάκτης: Addison-Wesley Iberoamericana.
- PubChem. (2019). Κυκλοεξένιο. Ανακτήθηκε από: pubchem.ncbi.nlm.nih.gov
- Chemical Book. (2019). Κυκλοεξένιο. Ανακτήθηκε από: chembook.com
- Δίκτυο δεδομένων τοξικολογίας. (2017). Κυκλοεξένιο. Toxnet Ανακτήθηκε από: toxnet.nlm.nih.gov
- Chemoxy. (s.f.). Ο δομικός τύπος για το κυκλοεξένιο είναι. Ανακτήθηκε από: chemoxy.com


