Δομή δισανθρακικού ασβεστίου, ιδιότητες, κίνδυνοι και χρήσεις
Το δισανθρακικό ασβέστιο είναι ένα ανόργανο άλας με χημικό τύπο Ca (HCO)3)2. Προέρχεται από τη φύση του από το ανθρακικό ασβέστιο που υπάρχει στα ασβεστολιθικά πετρώματα και στα ορυκτά όπως το ασβεστίτη.
Το δισανθρακικό ασβέστιο είναι περισσότερο διαλυτό στο νερό από το ανθρακικό ασβέστιο. Αυτό το χαρακτηριστικό έχει επιτρέψει το σχηματισμό καρστικών συστημάτων σε ασβεστολιθικούς βράχους και στη δομή σπηλαίων.

Τα υπόγεια ύδατα που διέρχονται από τις ρωγμές καθίστανται κορεσμένα με την εκτόπισή τους διοξειδίου του άνθρακα (CO2). Αυτά τα νερά διαβρώνουν τους ασβεστολιθικούς βράχους που απελευθερώνουν ανθρακικό ασβέστιο (CaCO3) που θα σχηματίσουν το όξινο ανθρακικό ασβέστιο, σύμφωνα με την ακόλουθη αντίδραση:
CaCO3(ες) + CO2(g) + Η2O (1) => Ca (HCO)3)2(aq)
Η αντίδραση αυτή συμβαίνει σε σπηλιές όπου προέρχεται πολύ σκληρό νερό. Το διττανθρακικό ασβέστιο δεν βρίσκεται στη στερεά κατάσταση αλλά σε ένα υδατικό διάλυμα μαζί με το Ca2+, το όξινο ανθρακικό (HCO)3-) και το ανθρακικό ιόν (CO32-).
Στη συνέχεια, όταν ο κορεσμός του διοξειδίου του άνθρακα στο νερό μειώνεται, συμβαίνει η αντίστροφη αντίδραση, δηλαδή ο μετασχηματισμός του όξινου ανθρακικού ασβεστίου σε ανθρακικό ασβέστιο:
Ca (HCO)3)2(aq) => CO2 (g) + Η2O (1) + CaCO3 (ες)
Το ανθρακικό ασβέστιο είναι ελάχιστα διαλυτό στο νερό, γεγονός που προκαλεί την καθίζησή του ως στερεό. Η παραπάνω αντίδραση είναι πολύ σημαντική για το σχηματισμό σταλακτιτών, σταλαγμιτών και άλλων σπηλαιώμων σε σπηλιές.
Αυτές οι βραχώδεις κατασκευές σχηματίζονται από τις σταγόνες νερού που πέφτουν από το ανώτατο όριο των σπηλαίων (κορυφή εικόνα). Το CaCO3 που υπάρχει στις σταγόνες νερού κρυσταλλώνεται για να σχηματίσει τις αναφερόμενες δομές.
Το γεγονός ότι το όξινο ανθρακικό ασβέστιο δεν βρίσκεται στη στερεά κατάσταση έχει κάνει τη χρήση του δύσκολη και λίγα παραδείγματα βρίσκονται. Επίσης, είναι δύσκολο να βρεθούν πληροφορίες για τις τοξικές επιδράσεις του. Υπάρχει μια αναφορά για μια σειρά παρενεργειών της χρήσης της ως θεραπεία για την πρόληψη της οστεοπόρωσης.
Δομή
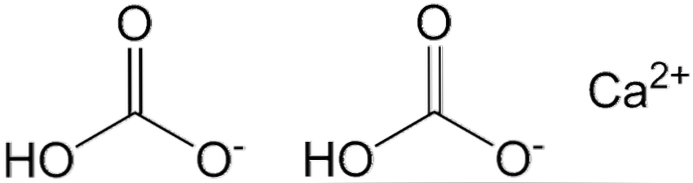
Δύο HCO ανιόντα εμφανίζονται στην επάνω εικόνα3- και ένα κατιόν2+ αλληλεπιδρώντας ηλεκτροστατικά. Το Ca2+ σύμφωνα με την εικόνα, θα πρέπει να βρίσκεται στη μέση, δεδομένου ότι έτσι είναι οι HCOs3- δεν θα απέφευγαν ο ένας τον άλλο λόγω των αρνητικών τους επιβαρύνσεων.
Η αρνητική επιβάρυνση στο HCO3- μετατοπίζεται μεταξύ δύο ατόμων οξυγόνου, με συντονισμό μεταξύ της καρβοξυλομάδας C = O και του δεσμού C-O-? ενώ στο CO32-, Αυτό μετατοπίζεται μεταξύ των τριών ατόμων οξυγόνου, αφού ο δεσμός Ο-ΟΗ αποπρωτονώνεται και μπορεί επομένως να λάβει ένα αρνητικό φορτίο με συντονισμό.
Οι γεωμετρίες αυτών των ιόντων μπορούν να θεωρηθούν ως σφαίρες ασβεστίου που περιβάλλεται από επίπεδα τριγωνικά ανθρακικά άλατα με υδρογονωμένο άκρο. Όσον αφορά την αναλογία μεγέθους, το ασβέστιο είναι αισθητά μικρότερο από τα ιόντα HCO3-.
Υδατικά διαλύματα
Το Ca (HCO)3)2 Δεν μπορεί να σχηματίσει κρυσταλλικά στερεά, και πραγματικά αποτελείται από υδατικά διαλύματα αυτού του άλατος. Σε αυτά, τα ιόντα δεν είναι μόνοι, όπως στην εικόνα, αλλά περιβάλλεται από μόρια Η.2Ο.
Πώς αλληλεπιδρούν; Κάθε ιόν περιβάλλεται από μια σφαίρα ενυδάτωσης, η οποία εξαρτάται από το μέταλλο, την πολικότητα και τη δομή των διαλελυμένων ειδών.
Το Ca2+ συντονίζει με τα άτομα οξυγόνου του νερού για να σχηματίσει ένα υδατοστοιχείο, το Ca (OH)2)n2+, όπου η γενικά θεωρείται ότι είναι έξι. δηλαδή ένα "υδατικό οκταεδρόν" γύρω από το ασβέστιο.
Ενώ ανιόντα HCO3- αλληλεπιδρούν είτε με δεσμούς υδρογόνου (OR2CO-Η-ΟΗ2) ή με τα άτομα υδρογόνου στο νερό προς την κατεύθυνση του αρνητικού φορτίου απομακρύνεται (HOCO)2- Η-ΟΗ, αλληλεπίδραση διπολικού ιόντος).
Αυτές οι αλληλεπιδράσεις μεταξύ του Ca2+, HCO3- και το νερό είναι τόσο αποτελεσματικό, ώστε να καταστήσει το όξινο ανθρακικό ασβέστιο πολύ διαλυτό σε αυτόν τον διαλύτη. σε αντίθεση με το CaCO3, στην οποία τα ηλεκτροστατικά αξιοθέατα μεταξύ του Ca2+ και το CO32- είναι πολύ ισχυρές, κατακρημνισμένες από το υδατικό διάλυμα.
Εκτός από το νερό, υπάρχουν μόρια CO2 γύρω, τα οποία αντιδρούν αργά για να παρέχουν περισσότερα HCO3- (ανάλογα με τις τιμές pH).
Υποθετικό στερεό
Μέχρι στιγμής, τα μεγέθη και τα φορτία των ιόντων στο Ca (HCO)3)2, ούτε η παρουσία νερού, να εξηγήσει γιατί η στερεά ένωση δεν υπάρχει? που είναι καθαροί κρύσταλλοι που μπορούν να χαρακτηριστούν με κρυσταλλογραφία ακτίνων Χ. Το Ca (HCO)3)2 δεν είναι τίποτα περισσότερο από τα ιόντα που υπάρχουν στο νερό από το οποίο οι σπηλαιώδεις σχηματισμοί συνεχίζουν να αναπτύσσονται.
Ναι Ca2+ και το HCO3- θα μπορούσαν να απομονωθούν από το νερό αποφεύγοντας την ακόλουθη χημική αντίδραση:
Ca (HCO)3)2(υδ) → CaCO3(ες) + CO2(g) + Η2O (l)
Τότε αυτά θα μπορούσαν να ομαδοποιηθούν σε ένα λευκό κρυσταλλικό στερεό με στοιχειομετρικές αναλογίες 2: 1 (2ΗΟΟ3/ 1Ca). Δεν υπάρχουν μελέτες σχετικά με τη δομή του, αλλά θα μπορούσε να συγκριθεί με το NaHCO3 (για διττανθρακικό μαγνήσιο, Mg (HCO)3)2, ούτε υπάρχει ως στερεό), ή με το CaCO3.
Σταθερότητα: NaHCO3 vs Ca (HCO)3)2
Το NaHCO3 κρυσταλλώνεται στο μονοκλινικό σύστημα και το CaCO3 στα τριγωνικά (ασβεστούχα) και ορθορομβικά (αραγωνίτης) συστήματα. Αν το Na αντικατασταθεί+ για το Ca2+, το κρυσταλλικό δίκτυο θα αποσταθεροποιηθεί από τη μεγαλύτερη διαφορά στα μεγέθη. δηλαδή, το Na+ επειδή είναι μικρότερο, σχηματίζει έναν πιο σταθερό κρύσταλλο με το HCO3- σε σύγκριση με το Ca2+.
Στην πραγματικότητα, το Ca (HCO)3)2(aq) χρειάζεται το νερό να εξατμιστεί έτσι ώστε τα ιόντα του να μπορούν να ομαδοποιηθούν σε ένα κρύσταλλο. αλλά το κρυσταλλικό πλέγμα αυτού του δεν είναι αρκετά ισχυρό για να το κάνει σε θερμοκρασία δωματίου. Όταν θερμαίνεται το νερό, λαμβάνει χώρα η αντίδραση αποσύνθεσης (παραπάνω εξίσωση).
Όντας το ιόν Na+ σε διάλυμα, αυτό θα σχηματίσει τον κρύσταλλο με το HCO3- πριν από τη θερμική αποσύνθεση.
Ο λόγος λοιπόν γιατί ο Ca (HCO)3)2 δεν κρυσταλλώνει (θεωρητικά), είναι με τη διαφορά των ιοντικών ακτίνων ή των μεγεθών των ιόντων του, τα οποία δεν μπορούν να σχηματίσουν έναν σταθερό κρύσταλλο πριν από την αποσύνθεσή του.
Ca (HCO)3)2 vs CaCO3
Εάν, από την άλλη πλευρά, προστέθηκε το Η+ στις κρυσταλλικές δομές του CaCO3, θα άλλαζαν δραστικά τις φυσικές τους ιδιότητες. Ίσως, τα σημεία τήξης της πέφτουν αισθητά και ακόμη και οι μορφολογίες των κρυστάλλων καταλήγουν να τροποποιούνται.
Θα αξίζει να δοκιμάσετε τη σύνθεση του Ca (HCO)3)2 στερεά; Οι δυσκολίες μπορεί να υπερβαίνουν τις προσδοκίες και ένα άλας με χαμηλή δομική σταθερότητα μπορεί να μην προσφέρει σημαντικά πρόσθετα οφέλη σε οποιαδήποτε εφαρμογή όπου ήδη χρησιμοποιούνται άλλα άλατα.
Φυσικές και χημικές ιδιότητες
Χημικός τύπος
Ca (HCO)3)2
Μοριακό βάρος
162,11 g / mol
Φυσική κατάσταση
Δεν εμφανίζεται σε στερεή κατάσταση. Βρίσκεται σε υδατικό διάλυμα και επιχειρεί να μετατραπεί σε στερεό με εξάτμιση νερού, δεν έχει εργαστεί καθώς μετατρέπεται σε ανθρακικό ασβέστιο.
Διαλυτότητα στο νερό
16,1 g / 100 ml στους 0 ° C. 16,6 g / 100 ml στους 20 ° C και 18,4 g / 100 ml στους 100 ° C. Αυτές οι τιμές είναι ενδεικτικές μιας υψηλής συγγένειας των μορίων ύδατος για ιόντα Ca (HCO)3)2, όπως εξηγείται στην προηγούμενη ενότητα. Εν τω μεταξύ, μόνο 15 mg CaCO3 διαλύονται σε ένα λίτρο νερού, γεγονός που αντανακλά τις ισχυρές ηλεκτροστατικές αλληλεπιδράσεις τους.
Επειδή το Ca (HCO)3)2 δεν μπορεί να σχηματίσει ένα στερεό, η διαλυτότητα του δεν μπορεί να προσδιοριστεί πειραματικά. Ωστόσο, δεδομένων των συνθηκών που δημιουργούνται από την CO2 διαλυμένο στο νερό που περιβάλλει τον ασβεστόλιθο, η μάζα του ασβεστίου διαλυμένη σε θερμοκρασία Τ θα μπορούσε να υπολογιστεί. μάζα, η οποία θα ήταν ίση με τη συγκέντρωση Ca (HCO)3)2.
Σε διαφορετικές θερμοκρασίες, η διαλυμένη μάζα αυξάνεται όπως φαίνεται από τις τιμές στους 0, 20 και 100 ° C. Έτσι, σύμφωνα με αυτά τα πειράματα, πόσο από το Ca (HCO) προσδιορίζεται3)2 διαλύεται στην περιοχή του CaCO3 σε ένα υδατικό μέσο αεριοποιημένο με CO2. Μόλις διαφύγει το CO2 αέρια, το CaCO3 θα καταβυθιστεί, αλλά όχι το Ca (HCO3)2.
Σημεία σύντηξης και βρασμού
Το κρυσταλλικό δίκτυο του Ca (HCO)3)2 είναι πολύ ασθενέστερο από το CaCO3. Εάν μπορεί να ληφθεί σε στερεή κατάσταση και να μετρηθεί η θερμοκρασία με την οποία τήκεται μέσα σε ένα πυροσθόμετρο, θα πήγαινε σίγουρα μια τιμή αρκετά κάτω από 899ºC. Ομοίως, το ίδιο θα μπορούσε να αναμένεται και στον προσδιορισμό του σημείου ζέσεως.
Σημείο καύσης
Δεν είναι καύσιμο.
Κίνδυνοι
Επειδή αυτή η ένωση δεν υπάρχει σε στερεή μορφή, είναι απίθανο να αντιπροσωπεύει έναν κίνδυνο χειρισμού των υδατικών διαλυμάτων της, καθώς τόσο το Ca2+ ως HCO3- δεν είναι επιβλαβείς σε χαμηλές συγκεντρώσεις. και ως εκ τούτου, ο μεγαλύτερος κίνδυνος που θα επωφελούνταν από τέτοιες λύσεις, θα μπορούσε να οφείλεται μόνο σε μια επικίνδυνη δόση ασβεστίου που καταναλώθηκε.
Αν η ένωση σχηματίσει ένα στερεό, παρόλο που μπορεί να είναι φυσικά διαφορετικό από το CaCO3, οι τοξικές του επιδράσεις δεν πρέπει να υπερβαίνουν την απλή δυσφορία και τις εκτομές μετά από φυσική επαφή ή εισπνοή.
Χρησιμοποιεί
-Τα διαλύματα διττανθρακικού ασβεστίου έχουν χρησιμοποιηθεί για μεγάλο χρονικό διάστημα για να πλύνουν παλιά έγγραφα, ειδικά έργα τέχνης ή ιστορικά σημαντικά έγγραφα.
-Η χρήση διττανθρακικών διαλυμάτων είναι χρήσιμη, όχι μόνο επειδή εξουδετερώνουν τα οξέα στο χαρτί, αλλά επίσης παρέχει ένα αλκαλικό απόθεμα ανθρακικού ασβεστίου. Αυτή η τελευταία σύνθεση παρέχει προστασία για μελλοντικές ζημιές στο χαρτί.
-Όπως και άλλα διττανθρακικά, χρησιμοποιείται σε χημικές ζυμομύκητες και στις συνθέσεις αναβράζοντων δισκίων ή σκονών. Επιπλέον, το όξινο ανθρακικό ασβέστιο χρησιμοποιείται ως πρόσθετο τροφίμων (υδατικά διαλύματα αυτού του άλατος).
-Τα διττανθρακικά διαλύματα έχουν χρησιμοποιηθεί στην πρόληψη της οστεοπόρωσης. Ωστόσο, σε μία περίπτωση παρατηρήθηκαν δευτερογενείς επιδράσεις όπως η υπερασβεστιαιμία, η μεταβολική αλκάλωση και η νεφρική ανεπάρκεια..
-Το δισανθρακικό ασβέστιο χορηγείται, περιστασιακά, ενδοφλέβια για να διορθώσει το καταθλιπτικό αποτέλεσμα της υποκαλιαιμίας στην καρδιακή λειτουργία.
-Και τέλος, παρέχει ασβέστιο στο σώμα, το οποίο είναι μεσολαβητής της σύσπασης των μυών, ενώ ταυτόχρονα διορθώνει την οξέωση που μπορεί να εμφανιστεί σε μια κατάσταση υποκαλιαιμίας..
Αναφορές
- Wikipedia. (2018). Διττανθρακικό ασβέστιο. Λαμβάνεται από: en.wikipedia.org
- Σίρα Ντουμπάις. (3 Οκτωβρίου 2017). Τι είναι το Bicarbonate του ασβεστίου; Ανακτήθηκε από: livestrong.com
- Επιστημονικό Κέντρο Μάθησης. (2018). Χημεία ανθρακικών αλάτων. Ανακτήθηκε από: sciencelearn.org.nz
- PubChem. (2018). Βυανθρακικό ασβέστιο. Ανακτήθηκε από: pubchem.ncbi.nlm.nih.gov
- Amy Ε. Gerbracht & Irene Brückle. (1997). Η Χρήση των Διαλυμάτων Βικαρβονικού Ασβεστίου και Διττανθρακικού Μαγνησίου σε Μικρά Εργαστήρια Συντήρησης: Αποτελέσματα Έρευνας. Ανακτήθηκε από: cool.conservation-us.org


