Ιδιότητες ιωδίου καλίου, δομή, χρήσεις και κίνδυνοι
Το ιωδιούχο κάλιο ή ιωδιούχο κάλιο είναι μια ανόργανη ένωση του ιωδίου, συγκεκριμένα ένα άλας, του οποίου ο χημικός τύπος είναι ΚΙΟ3. Το ιώδιο, στοιχείο της ομάδας αλογόνων (F, CI, Br, I, As), έχει σε αυτό το άλας αριθμό οξείδωσης +5. λόγω αυτού είναι ένας ισχυρός παράγοντας οξείδωσης. Το ΚΙΟ3 διασπάται σε υδατικό μέσο για να δημιουργήσει τα ιόντα Κ+ και IO3-.
Συντίθεται με αντίδραση υδροξειδίου του καλίου με ιωδιούχο οξύ: HIO3(υδ) + ΚΟΗ (s) => ΚΙΟ3(υδ) + Η2O (l) Επίσης, μπορεί να συντεθεί με αντίδραση μοριακού ιωδίου με υδροξείδιο καλίου: 3Ι2(s) + 6ΚΟΗ (s) => ΚΙΟ3(υδατ.) + 5Κΐ (υδατ.) + 3Η2O (l).

Ευρετήριο
- 1 Φυσικές και χημικές ιδιότητες
- 1.1 Οξειδωτικός παράγων
- 2 Χημική δομή
- 3 Χρήσεις και εφαρμογές ιωδιούχου καλίου
- 3.1 Θεραπευτική χρήση
- 3.2 Χρήση στη βιομηχανία
- 3.3 Αναλυτική χρήση
- 3.4 Χρήση σε τεχνολογία λέιζερ
- 4 Κίνδυνοι για την υγεία του ιωδικού καλίου
- 5 Αναφορές
Φυσικές και χημικές ιδιότητες
Πρόκειται για άοσμο λευκό στερεό, με λεπτούς κρυστάλλους και κρυσταλλική δομή μονοκλινικού τύπου. Έχει πυκνότητα 3,98 g / ml, μοριακό βάρος 214 g / mol και έχει ζώνες απορρόφησης στο υπέρυθρο (IR) φάσμα.
Έχει σημείο τήξης: 833 K (560 ºC), σύμφωνα με τις ισχυρές ιονικές αλληλεπιδράσεις μεταξύ των ιόντων K+ και IO3-. Σε υψηλότερες θερμοκρασίες, υφίσταται μια αντίδραση θερμικής αποσύνθεσης, απελευθερώνοντας μοριακό οξυγόνο και ιωδιούχο κάλιο:
2KIO3(s) => 2KI + 3O2(ζ)
Έχει διαλυτότητες στο νερό που κυμαίνεται από 4,74g / 100mL έως 0 ° C, έως 32,3 g / 100 mL έως 100 ° C, δημιουργώντας άχρωμα υδατικά διαλύματα. Επιπλέον, είναι αδιάλυτο σε αλκοόλη και νιτρικό οξύ, αλλά είναι διαλυτό σε αραιό θειικό οξύ.
Η συγγένειά του με το νερό δεν είναι αξιόλογη, γεγονός που εξηγεί γιατί δεν είναι υγροσκοπικό και δεν υπάρχει υπό τη μορφή ενυδατωμένων αλάτων (KIO)3· H2Ο).
Οξειδωτικό μέσο
Το ιωδιούχο κάλιο, όπως φαίνεται από τον χημικό τύπο του, έχει τρία άτομα οξυγόνου. Αυτό είναι ένα έντονα ηλεκτροαρνητικό στοιχείο και, λόγω αυτής της ιδιότητας, «αποκαλύπτει» μια ηλεκτρονική ανεπάρκεια στο σύννεφο γύρω από το ιώδιο.
Αυτή η ανεπάρκεια, ή εισόδου, όπως την περίπτωση- μπορεί να υπολογιστεί ως ο αριθμός οξείδωσης του ιωδίου (± 1, +2, +3, +5, +7), όντας +5 στην περίπτωση αυτού του άλατος.
Τι σημαίνει αυτό; Ότι πριν από ένα είδος ικανό να αποδώσει τα ηλεκτρόνια του, το ιώδιο θα τα δεχτεί σε ιοντική μορφή (IO3-) για να γίνει μοριακό ιώδιο και να έχει αριθμό οξείδωσης ίσο με 0.
Μετά από αυτή την εξήγηση μπορεί να προσδιοριστεί ότι το ιωδικό κάλιο είναι μια οξειδωτική ένωση που αντιδρά ισχυρά με αναγωγικούς παράγοντες σε πολλές οξειδοαναγωγικές αντιδράσεις. από όλα αυτά, το ένα είναι γνωστό ως ρολόι ιωδίου.
Το ρολόι ιωδίου αποτελείται από μια διαδικασία οξειδοαναγωγής αργών και γρήγορων βημάτων, στην οποία τα γρήγορα βήματα χαρακτηρίζονται από μια λύση KIO3 σε θειικό οξύ στο οποίο προστίθεται άμυλο. Στη συνέχεια, το άμυλο - όταν παράγεται και αγκυροβοληθεί μεταξύ των ειδών δομής του3-- θα μετατρέψει το διάλυμα από άχρωμο σε σκούρο μπλε.
IO3- + 3 HSO3- → εγώ- + 3 HSO4-
IO3- + 5 Ι- + 6 Η+ → 3 Ι2 + 3 Η2Ο
Εγώ2 + HSO3- + H2O → 2 I- + HSO4- + 2 Η+ (σκούρο μπλε λόγω επίδρασης αμύλου)
Χημική δομή
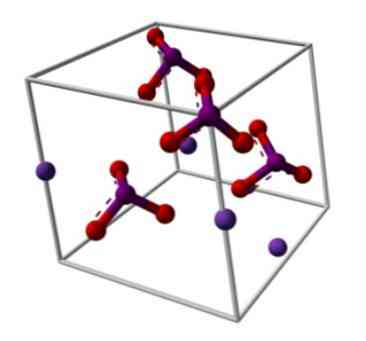
Η χημική δομή του ιωδιούχου καλίου απεικονίζεται στην άνω εικόνα. Το ανιόν ΙΟ3- αντιπροσωπεύεται από το "τρίποδο" των κόκκινων και μοβ σφαιριδίων, ενώ τα Κ ιόντα+ αντιπροσωπεύονται από τις μοβ σφαίρες.
Αλλά τι σημαίνουν αυτά τα τρίποδα; Οι σωστές γεωμετρικά σχήματα από αυτά τα ανιόντα είναι πραγματικά τριγωνική πυραμίδες, στην οποία οι οξυγόνα σχηματίζουν την τριγωνική βάση, και το μεμονωμένο ζεύγος των σημείων ηλεκτρονίων ιωδίου προς τα πάνω, καταλαμβάνοντας χώρο και αναγκάζοντας φορές κάτω από το σύνδεσμο IO και τα δύο συνδέσεις I = O.
Αυτή η μοριακή γεωμετρία αντιστοιχεί σε μια υβριδοποίηση sp3 του κεντρικού ατόμου ιωδίου. Ωστόσο, μια άλλη προοπτική υποδεικνύει ότι ένα από τα άτομα οξυγόνου σχηματίζει δεσμούς με τα «d» τροχιακά του ιωδίου, πράγματι είναι ένας υβριδισμός sp3δ2 (το ιώδιο μπορεί να έχει τις τροχιές του "d" να επεκτείνει το κέλυφος σθένους του).
Οι κρύσταλλοι αυτού του αλατιού μπορούν να υποστούν μεταβολές της δομικής φάσης (άλλες ρυθμίσεις από τις μονοκλινικές) ως συνέπεια των διαφορετικών φυσικών συνθηκών που τους υπόκεινται.
Χρήσεις και εφαρμογές ιωδιούχου καλίου
Θεραπευτική χρήση
Το ιωδιούχο κάλιο χρησιμοποιείται συνήθως για την πρόληψη της συσσώρευσης ραδιενέργειας στον θυρεοειδή με τη μορφή του 131Ι, όταν αυτό το ισότοπο χρησιμοποιείται στον προσδιορισμό της πρόσληψης ιωδίου από τον θυρεοειδή ως συστατικό της λειτουργίας του θυρεοειδούς αδένα.
Ομοίως, το ιωδιούχο κάλιο χρησιμοποιείται ως τοπικό αντισηπτικό (0,5%) στις λοιμώξεις του βλεννογόνου.
Χρήση στη βιομηχανία
Προστίθεται στη ζωοτροφή των αγροτικών ζώων ως συμπλήρωμα ιωδίου. Ως εκ τούτου, στον κλάδο χρησιμοποιείται ιωδιούχο κάλιο για τη βελτίωση της ποιότητας των αλεύρων.
Αναλυτική χρήση
Στην αναλυτική χημεία, χάρη στη σταθερότητά του, χρησιμοποιείται ως πρωταρχικό πρότυπο στην τυποποίηση των προτύπων διαλυμάτων θειοθειικού νατρίου (Na2S2Ο3), προκειμένου να προσδιοριστούν οι συγκεντρώσεις ιωδίου στα δείγματα.
Αυτό σημαίνει ότι οι ποσότητες ιωδίου μπορούν να είναι γνωστές με ογκομετρικές τεχνικές (τιτλοδοτήσεις). Σε αυτή την αντίδραση, το ιωδιούχο κάλιο οξειδώνει τα ιόντα ιωδίου Ι ταχέως-, με την ακόλουθη χημική εξίσωση:
IO3- + 5Ι- + 6Η+ => 3Ι2 + 3Η2Ο
Ιώδιο, εγώ2, τιτλοδοτείται με το διάλυμα Na2S2Ο3 για την τυποποίησή του.
Χρησιμοποιείται στην τεχνολογία λέιζερ
Μελέτες έχουν δείξει και επιβεβαιώθηκε ενδιαφέρουσες πιεζοηλεκτρικές ιδιότητες, πυροηλεκτρικό, ηλεκτροπτικών, κρύσταλλοι φερροηλεκτρικού και μη γραμμικές οπτικές KIO3. Αυτό έχει ως αποτέλεσμα μεγάλες δυνατότητες στο ηλεκτρονικό πεδίο και στην τεχνολογία των λέιζερ για υλικά που κατασκευάζονται με αυτή την ένωση.
Κίνδυνοι για την υγεία του ιωδικού καλίου
Σε υψηλές δόσεις μπορεί να προκαλέσει ερεθισμό στον βλεννογόνο του στόματος, στο δέρμα, στα μάτια και στην αναπνευστική οδό.
Πειράματα της τοξικότητας ιωδικού καλίου σε ζώα επέτρεψαν να παρατηρήσουμε ότι σε νηστεία σκύλους σε δόσεις από 0,2 έως 0,25 g / kg σωματικού βάρους, χορηγούνται από του στόματος, προκαλεί εμετό ένωση.
Αν αποφευχθούν αυτοί οι εμετείς, προκαλεί επιδείνωση της κατάστασης στα ζώα, καθώς προκαλεί ανορεξία και προσβολή πριν από το θάνατο. Οι αυτοψίες του επέτρεψαν να παρατηρήσουν νεκρωτικές αλλοιώσεις στο ήπαρ, τα νεφρά και τον εντερικό βλεννογόνο.
Λόγω της οξειδωτικής του ισχύος, αντιπροσωπεύει κίνδυνο πυρκαγιάς όταν έρχεται σε επαφή με εύφλεκτα υλικά.
Αναφορές
- Ημέρα, R., & Underwood, Α. Ποσοτική Αναλυτική Χημεία (πέμπτη έκδοση). PEARSON Prentice Hall, ρ-364.
- Muth, D. (2008). Λέιζερ [Εικόνα]. Ανακτήθηκε από: flickr.com
- ChemicalBook. (2017). Ιωδικό κάλιο. Ανακτήθηκε στις 25 Μαρτίου 2018, από την ChemicalBook: chemicalbook.com
- PubChem. (2018). Ιωδικό κάλιο. Ανακτήθηκε στις 25 Μαρτίου 2018, από την PubChem: pubchem.ncbi.nlm.nih.gov
- Merck. (2018). Ιωδικό κάλιο. Ανακτήθηκε στις 25 Μαρτίου 2018, από τη Merck:
- merckmillipore.com
- Wikipedia. (2017). Ιωδικό κάλιο. Ανακτήθηκε στις 25 Μαρτίου 2018, από τη Wikipedia: en.wikipedia.org
- Μ Μ Abdel Kader et αϊ. (2013). Μηχανισμός μεταφοράς φορτίου και μεταβατικές φάσεις χαμηλής θερμοκρασίας στο KIO3. J. Phys .: Conf. Ser. 423 012036


