Οξείδια του αζώτου (NOx) Διαφορετικά σκευάσματα και ονοματολογίες
Το οξείδια του αζώτου είναι ουσιαστικά αέριες ανόργανες ενώσεις που περιέχουν δεσμούς μεταξύ ατόμων αζώτου και οξυγόνου. Ο χημικός τύπος της ομάδας του είναι ΟΧΙx, υποδεικνύοντας ότι τα οξείδια έχουν διαφορετικές αναλογίες οξυγόνου και αζώτου.
Το άζωτο οδηγεί την ομάδα 15 του περιοδικού πίνακα, ενώ η ομάδα οξυγόνου 16, και τα δύο στοιχεία είναι μέλη της περιόδου 2. Αυτή η εγγύτητα είναι ο λόγος για τον οποίο οι δεσμοί Ν-Ο είναι ομοιοπολικοί στα οξείδια. Με τον τρόπο αυτό, οι δεσμοί στα οξείδια του αζώτου είναι ομοιοπολικοί.
Όλοι αυτοί οι σύνδεσμοι μπορούν να εξηγηθούν χρησιμοποιώντας τη θεωρία του μοριακού τροχιακού, ο οποίος αποκαλύπτει τον παραμαγνητισμό (ένα ηλεκτρόνιο μη συζευγμένο στο τελευταίο μοριακό τροχιακό) μερικών από αυτές τις ενώσεις. Από αυτές, οι πιο κοινές ενώσεις είναι το νιτρικό οξείδιο και το διοξείδιο του αζώτου.
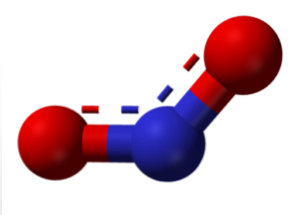
Το μόριο στην άνω εικόνα αντιστοιχεί στη γωνιακή δομή διοξειδίου του αζώτου (NO2). Αντίθετα, το μονοξείδιο του αζώτου (ΝΟ) έχει γραμμική δομή (θεωρώντας τον υβ υβριδισμό και για τα δύο άτομα).
Τα οξείδια του αζώτου είναι αέρια που παράγονται από πολλές ανθρώπινες δραστηριότητες, από την οδήγηση οχήματος ή το κάπνισμα τσιγάρων, σε βιομηχανικές διεργασίες ως ρυπογόνα απόβλητα. Ωστόσο, το ΝΟ παράγεται φυσικά με ενζυματικές αντιδράσεις και κεραυνό στις καταιγίδες: Ν2(g) + Ο2(g) => 2ΝΟ (g)
Οι υψηλές θερμοκρασίες των ακτίνων σπάνε το ενεργειακό φράγμα που εμποδίζει αυτή την αντίδραση να εμφανιστεί υπό κανονικές συνθήκες. Ποιο ενεργειακό φράγμα; Αυτό σχηματίστηκε από τον τριπλό δεσμό N≡N, κάνοντας το Ν-μόριο2 ένα αδρανές αέριο από την ατμόσφαιρα.
Ευρετήριο
- 1 Οξείδωση αριθμών για το άζωτο και το οξυγόνο στα οξείδια τους
- 2 Διαφορετικές συνταγές και ονοματολογίες
- 2.1 Οξείδιο του αζώτου (N2O)
- 2.2 Μονοξείδιο του αζώτου (ΝΟ)
- 2.3 Τριοξείδιο του αζώτου (N2O3)
- 2.4 Διοξείδιο και τετροξείδιο του αζώτου (NO2, N2O4)
- 2.5 Πεντοξείδιο δινιτρογόνου (N2O5)
- 3 Αναφορές
Αριθμοί οξείδωσης για το άζωτο και το οξυγόνο στα οξείδια τους
Η ηλεκτρονική διαμόρφωση για το οξυγόνο είναι [He] 2s22ρ4, χρειάζεται μόνο δύο ηλεκτρόνια για να ολοκληρώσει την οκτάδα του κελύφους του σθένους. δηλαδή, μπορεί να κερδίσει δύο ηλεκτρόνια και να έχει έναν αριθμό οξείδωσης ίσο με -2.
Από την άλλη πλευρά, η ηλεκτρονική διαμόρφωση για το άζωτο είναι [He] 2s22ρ3, να είναι σε θέση να κερδίσει έως και τρία ηλεκτρόνια για να γεμίσει την οκτάδα του σθένους. για παράδειγμα, στην περίπτωση της αμμωνίας (ΝΗ3) έχει έναν αριθμό οξείδωσης ίσο με -3. Αλλά το οξυγόνο είναι πολύ πιο ηλεκτροαρνητικό από το υδρογόνο και "αναγκάζει" το άζωτο να μοιράζεται τα ηλεκτρόνια του.
Πόσα ηλεκτρόνια μπορεί να μοιράζεται το άζωτο με οξυγόνο; Εάν μοιράζεστε τα ηλεκτρόνια του κελύφους σθένους σας μία προς μία, θα φτάσετε στο όριο των πέντε ηλεκτρονίων, που αντιστοιχεί σε έναν αριθμό οξείδωσης +5.
Κατά συνέπεια, ανάλογα με τον αριθμό των δεσμών που σχηματίζει με το οξυγόνο, οι αριθμοί οξείδωσης του αζώτου κυμαίνονται από +1 έως +5.
Διαφορετικές συνταγές και ονοματολογίες
Τα οξείδια του αζώτου, με αυξανόμενη σειρά αριθμών οξείδωσης αζώτου, είναι:
- Ν2Ή, το οξείδιο του αζώτου (+1)
- ΟΧΙ, νιτρικό οξείδιο (+2)
- Ν2Ο3, τριτοξείδιο του αζώτου (+3)
- Όχι2, διοξείδιο του αζώτου (+4)
- Ν2Ο5, πεντοξείδιο του αζώτου (+5)
Οξείδιο του αζώτου (Ν2Ο)
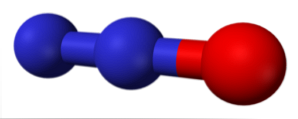
Το οξείδιο του αζώτου (ή ευρέως γνωστό ως αέριο γέλιου) είναι ένα άχρωμο αέριο, με μια ελαφρά γλυκιά οσμή και λίγο αντιδραστικό. Μπορεί να απεικονιστεί ως ένα μόριο Ν2 (μπλε σφαίρες) που έχει προσθέσει ένα άτομο οξυγόνου στο ένα άκρο. Παρασκευάζεται με τη θερμική αποσύνθεση νιτρικών αλάτων και χρησιμοποιείται ως αναισθητικό και αναλγητικό.
Το άζωτο έχει έναν αριθμό οξείδωσης +1 σε αυτό το οξείδιο, πράγμα που σημαίνει ότι δεν είναι πολύ οξειδωμένο και η ζήτησή του για ηλεκτρόνια δεν είναι επιτακτική. Ωστόσο, χρειάζεστε μόνο δύο ηλεκτρόνια (ένα για κάθε άζωτο) για να γίνει το σταθερό μοριακό άζωτο.
Σε βασικά και όξινα διαλύματα οι αντιδράσεις είναι:
Ν2O (g) + 2Η+(ac) + 2e- => Ν2(g) + Η2O (l)
Ν2O (g) + Η2O (1) + 2ε- => Ν2(g) + 2ΟΗ-(ac)
Αυτές οι αντιδράσεις, αν και θερμοδυναμικά ευνοούνται από το σχηματισμό του σταθερού μορίου Ν2, εμφανίζονται αργά και τα αντιδραστήρια που δίνουν το ζεύγος ηλεκτρονίων πρέπει να είναι πολύ ισχυροί αναγωγικοί παράγοντες.
Νιτρικό οξείδιο (ΝΟ)
Αυτό το οξείδιο αποτελείται από άχρωμο, αντιδραστικό και παραμαγνητικό αέριο. Όπως το νιτρώδες οξείδιο, έχει μια γραμμική μοριακή δομή, αλλά με τη μεγάλη διαφορά ότι ο δεσμός Ν = Ο έχει επίσης ένα χαρακτήρα τριπλού δεσμού..
Το ΝΟ οξειδώνεται ταχέως στον αέρα για να παράγει ΝΟ2, και έτσι να παράγουν πιο σταθερά μοριακά τροχιακά με περισσότερο οξειδωμένο άτομο αζώτου (+4).
2NO (g) + Ο2(g) => 2ΝΟ2(ζ)
Βιοχημικές και φυσιολογικές μελέτες βρίσκονται πίσω από τον καλοήθη ρόλο αυτού του οξειδίου σε ζωντανούς οργανισμούς.
Δεν μπορεί να σχηματίσει Ν-Ν δεσμούς με ένα άλλο μόριο ΝΟ λόγω της μετεγκατάστασης του μη ζευγαρωμένου ηλεκτρονίου στο μοριακό τροχιακό, το οποίο κατευθύνεται περισσότερο προς το άτομο οξυγόνου (λόγω της υψηλής ηλεκτρεναλλακτικότητας του). Το αντίθετο συμβαίνει με το NO2, που μπορεί να σχηματίσει αέρια διμερή.
Τριοξείδιο του αζώτου (Ν2Ο3)
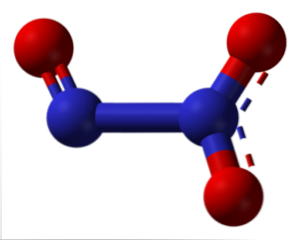
Οι διακεκομμένες γραμμές της δομής δείχνουν συντονισμό διπλού δεσμού. Όπως όλα τα άτομα, έχουν υβριδισμό sp2, το μόριο είναι επίπεδο και οι μοριακές αλληλεπιδράσεις είναι αρκετά αποτελεσματικές ώστε το τριοξείδιο του αζώτου να υπάρχει ως ένα μπλε στερεό κάτω από -101 ° C. Σε υψηλότερες θερμοκρασίες τήκεται και διασπάται σε NO και NO2.
Γιατί διαχωρίζεται; Επειδή οι αριθμοί οξείδωσης +2 και +4 είναι πιο σταθεροί από το +3, οι τελευταίοι υπάρχουν στο οξείδιο για καθένα από τα δύο άτομα αζώτου. Αυτό, πάλι, μπορεί να εξηγηθεί από τη σταθερότητα των μοριακών τροχιακών που προκύπτουν από τη δυσαναλογία.
Στην εικόνα, η αριστερή πλευρά του N2Ο3 αντιστοιχεί στο NO, ενώ η δεξιά πλευρά στο NO2. Λογικά, παράγεται από την συνένωση των προηγούμενων οξειδίων σε πολύ χαμηλές θερμοκρασίες (-20 ° C). Το Ν2Ο3 είναι ανυδρίτης νιτρώδους οξέος (ΗΝΟ2).
Διοξείδιο και τετροξείδιο του αζώτου (NO2, Ν2Ο4)
Όχι2 είναι ένα καφέ ή καφέ αέριο, αντιδραστικό και παραμαγνητικό. Δεδομένου ότι έχει ένα μη ζευγαρωμένο ηλεκτρόνιο, διμερίζεται (δεσμεύεται) με ένα άλλο NO αέριο μόριο2 για να σχηματίσουν τετροξείδιο του αζώτου, άχρωμο αέριο, δημιουργώντας μια ισορροπία μεταξύ των δύο χημικών ειδών:
2NO2(ζ) <=> Ν2Ο4(ζ)
Είναι ένας δηλητηριώδης και ευμετάβλητος οξειδωτικός παράγοντας, ικανός να δυσανάλογε στις οξειδοαναγωγικές του αντιδράσεις σε ιόντα (οξοανιόντα).2- και ΟΧΙ3- (δημιουργώντας όξινη βροχή), ή σε NO.
Ομοίως, το ΟΧΙ2 εμπλέκεται σε σύνθετες ατμοσφαιρικές αντιδράσεις που προκαλούν μεταβολές στις συγκεντρώσεις του όζοντος (OR3) σε χερσαία επίπεδα και στη στρατόσφαιρα.
Το πεντοξείδιο του αζώτου (N2Ο5)
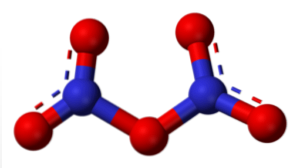
Όταν ενυδατώνεται, παράγει HNO3, και σε υψηλότερες συγκεντρώσεις του οξέος, το οξυγόνο κυρίως πρωτονιώνεται με μερικό θετικό φορτίο -0+-H, επιταχύνοντας τις αντιδράσεις οξειδοαναγωγής
Αναφορές
- αιτούντες. ((2006-2018)). αιτούντες. Ανακτήθηκε στις 29 Μαρτίου 2018 από τους αιτούντες: askiitians.com
- Encyclopaedia Britannica, Inc. (2018). Encyclopaedia Britannica. Ανακτήθηκε στις 29 Μαρτίου 2018, από την Encyclopaedia Britannica: britannica.com
- Tox Town. (2017). Tox Town. Ανακτήθηκε στις 29 Μαρτίου 2018, από το Tox Town: toxtown.nlm.nih.gov
- Καθηγήτρια Patricia Shapley. (2010). Οξείδια του αζώτου στην ατμόσφαιρα. Πανεπιστήμιο του Ιλινόις. Ανακτήθηκε στις 29 Μαρτίου 2018, από: butane.chem.uiuc.edu
- Shiver & Atkins. (2008). Ανόργανη χημεία Στο Τα στοιχεία της ομάδας 15. (Τέταρτη έκδοση, σελ. 361-366). Mc Graw Hill