Ατομικός τόμος Πώς διαφέρει στον περιοδικό πίνακα και τα παραδείγματα
Το ατομικού όγκου είναι μια σχετική τιμή που υποδεικνύει τη σχέση μεταξύ της μοριακής μάζας ενός στοιχείου και της πυκνότητας του. Επομένως, αυτός ο όγκος εξαρτάται από την πυκνότητα του στοιχείου και η πυκνότητα εξαρτάται με τη σειρά του από τη φάση και από τον τρόπο με τον οποίο τα άτομα είναι διευθετημένα μέσα σε αυτό.
Έτσι ώστε η ατομική όγκος για το στοιχείο Ζ δεν είναι ίση μέσα σε μια άλλη διακριτή φάση η οποία εμφανίζει σε θερμοκρασία δωματίου (υγρά, στερεά ή αέριο), ή όταν μέρος ορισμένων ενώσεων. Έτσι, η ατομική όγκος του Ζ στην ένωση ΖΑ είναι διαφορετική από Ζ στην ένωση ΖΒ.

Γιατί; Για να το καταλάβουμε, είναι απαραίτητο να συγκρίνουμε άτομα με, για παράδειγμα, μάρμαρα. Τα μάρμαρα, όπως τα γαλαζοπράσινα της ανώτερης εικόνας, έχουν πολύ καλά οριοθετήσει τα υλικά τους όρια, τα οποία παρατηρούνται χάρη στη λαμπρή επιφάνεια τους. Αντίθετα, τα όρια των ατόμων είναι διάχυτα, αν και μπορούν να θεωρηθούν μακρινά σφαιρικά.
Έτσι, αυτό που καθορίζει ένα σημείο πέρα από το ατομικό σύνορα είναι μηδέν πιθανότητα εύρεσης ένα ηλεκτρόνιο, και το σημείο αυτό θα μπορούσε να είναι περαιτέρω ή πιο κοντά στον πυρήνα ανάλογα με το πόσα γειτονικά άτομα αλληλεπιδρούν γύρω από το άτομο υπόψη.
Ευρετήριο
- 1 Ατομικός όγκος και ακτίνα
- 2 Πρόσθετος τύπος
- 3 Πώς διαφέρει ο ατομικός όγκος στον περιοδικό πίνακα?
- 3.1 Ατομικοί όγκοι μεταβατικών μετάλλων
- 4 Παραδείγματα
- 4.1 Παράδειγμα 1
- 4.2 Παράδειγμα 2
- 5 Αναφορές
Ατομικός όγκος και ακτίνα
Με την αλληλεπίδραση δύο ατόμων Η στο μόριο Η2, οι θέσεις των πυρήνων τους καθορίζονται καθώς και οι αποστάσεις μεταξύ τους (πυρηνικές αποστάσεις). Αν και τα δύο άτομα είναι σφαιρικά, η ακτίνα είναι η απόσταση μεταξύ του πυρήνα και του διάχυτου ορίου:
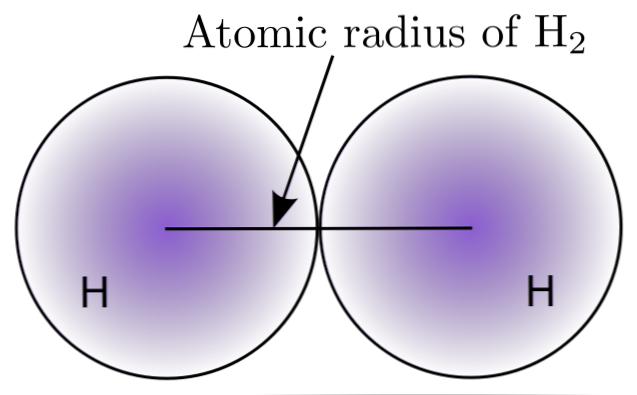
Στην άνω εικόνα μπορεί να δει κανείς πώς η πιθανότητα εύρεσης ενός ηλεκτρονίου μειώνεται καθώς απομακρύνεται από τον πυρήνα. Διαχωρίζοντας την πυρηνική απόσταση μεταξύ δύο, λαμβάνεται η ατομική ακτίνα. Στη συνέχεια, υποθέτοντας μια σφαιρική γεωμετρία για τα άτομα, χρησιμοποιούμε τον τύπο για να υπολογίσουμε τον όγκο μιας σφαίρας:
V = (4/3) (Pi) r3
Σε αυτή την έκφραση r είναι η ατομική ακτίνα που προσδιορίζεται για το μόριο Η2. Η τιμή του V που υπολογίζεται από αυτήν την ασαφή μέθοδο μπορεί να αλλάξει εάν, για παράδειγμα, θεωρήθηκε H2 σε υγρή ή μεταλλική κατάσταση. Ωστόσο, αυτή η μέθοδος είναι πολύ ανακριβής επειδή τα σχήματα των ατόμων είναι μακριά από την ιδανική σφαίρα στις αλληλεπιδράσεις τους.
Για τον προσδιορισμό των ατομικών τους όγκους των στερεών λαμβάνονται υπόψη πολλές μεταβλητές που αφορούν το καθεστώς, και οι μελέτες που λαμβάνονται με περίθλαση ακτίνων Χ.
Πρόσθετος τύπος
Η μοριακή μάζα εκφράζει την ποσότητα της ύλης που έχει ένα γραμμομόριο ατόμων ενός χημικού στοιχείου.
Οι μονάδες του είναι g / mol. Από την άλλη πλευρά, η πυκνότητα είναι ο όγκος που καταλαμβάνει ένα γραμμάριο του στοιχείου: g / mL. Επειδή οι μονάδες του ατομικού όγκου είναι mL / mol, πρέπει να παίξετε με τις μεταβλητές για να φτάσετε στις επιθυμητές μονάδες:
(g / mol) (ml / g) = mL / mol
Ή τι είναι το ίδιο:
(Μοριακή μάζα) (1 / D) = V
(Μοριακή μάζα / D) = V
Έτσι, ο όγκος ενός mole των ατόμων ενός στοιχείου μπορεί εύκολα να υπολογιστεί. ενώ με τον τύπο του σφαιρικού όγκου υπολογίζεται ο όγκος ενός μεμονωμένου ατόμου. Για να φτάσετε αυτή την τιμή από την πρώτη, απαιτείται μετατροπή μέσω του αριθμού του Avogadro (6.02 · 10).-23).
Πώς διαφέρει ο ατομικός όγκος στον περιοδικό πίνακα?
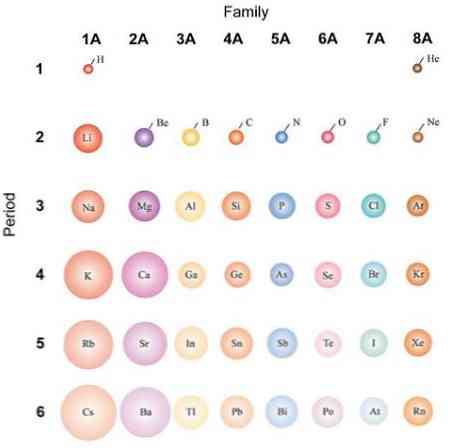
Αν τα άτομα θεωρηθούν σφαιρικά, τότε η παραλλαγή τους θα είναι ίδια με αυτά που παρατηρούνται σε ατομικές ακτίνες. Στην επάνω εικόνα, που δείχνει τα αντιπροσωπευτικά στοιχεία, απεικονίζεται ότι από τα δεξιά προς τα αριστερά τα άτομα είναι νάνοι. Αντίθετα, από πάνω προς τα κάτω αυτά γίνονται πιο ογκώδη.
Αυτό συμβαίνει επειδή στην ίδια περίοδο ο πυρήνας ενσωματώνει πρωτόνια καθώς κινείται προς τα δεξιά. Αυτά τα πρωτόνια ασκούν ελκυστική δύναμη στα εξωτερικά ηλεκτρόνια, τα οποία αισθάνονται ένα αποτελεσματικό πυρηνικό φορτίο Ζef, λιγότερο από το πραγματικό πυρηνικό φορτίο Ζ.
Τα ηλεκτρόνια των εσωτερικών στρώσεων απωθούν το εξωτερικό στρώμα, μειώνοντας την επίδραση αυτών των βασικών? Αυτό είναι γνωστό ως εφέ οθόνης. Κατά την ίδια περίοδο η επίδραση οθόνη αποτυγχάνει να αντισταθμίσει την αύξηση του αριθμού των πρωτονίων, έτσι ώστε τα ηλεκτρόνια του εσωτερικού στρώματος δεν εμποδίζουν συστολή των ατόμων.
Εντούτοις, κατεβαίνοντας σε μια ομάδα, ενεργοποιούνται νέα ενεργειακά επίπεδα, τα οποία επιτρέπουν στα ηλεκτρόνια να περνούν πιο μακριά από τον πυρήνα. Επίσης, ο αριθμός των ηλεκτρονίων στην εσωτερική στρώση αυξάνεται, των οποίων τα αποτελέσματα θωράκισης αρχίζουν να μειώνονται αν ο πυρήνας προσθέσει πάλι πρωτόνια.
Για τους λόγους αυτούς εκτιμάται ότι η ομάδα 1Α έχει τις bulkiest άτομα, σε αντίθεση με μικρών άτομα ομάδα 8Α (ή 18), το ευγενές αέριο.
Ατομικοί όγκοι μεταβατικών μετάλλων
Τα άτομα των μεταβατικών μετάλλων ενσωματώνουν ηλεκτρόνια στις εσωτερικές τροχιές d. Αυτή η αύξηση του αποτελέσματος της οθόνης και, όπως επίσης και του πραγματικού πυρηνικού φορτίου Z, ακυρώνονται σχεδόν εξίσου, έτσι ώστε τα άτομα τους να διατηρούν το ίδιο μέγεθος κατά την ίδια περίοδο.
Με άλλα λόγια: σε μια περίοδο, τα μεταβατικά μέταλλα παρουσιάζουν παρόμοιους ατομικούς όγκους. Ωστόσο, αυτές οι μικρές διαφορές είναι εξαιρετικά σημαντικές όταν καθορίζουμε τους μεταλλικούς κρυστάλλους (σαν να ήταν μεταλλικά μάρμαρα).
Παραδείγματα
Δύο μαθηματικοί τύποι είναι διαθέσιμοι για τον υπολογισμό του ατομικού όγκου ενός στοιχείου, ο καθένας με τα αντίστοιχα παραδείγματα.
Παράδειγμα 1
Λαμβάνοντας υπόψη την ατομική ακτίνα του υδρογόνου -37 μm (1 picometer = 10-12m) - και το καίσιο -265 pm-, υπολογίζει τους ατομικούς όγκους του.
Χρησιμοποιώντας τον τύπο του σφαιρικού όγκου, έχουμε στη συνέχεια:
VH= (4/3) (3,14) (37 μm)3= 212,07 pm3
VCs= (4/3) (3.14) (265 μ.μ.)3= 77912297,67 pm3
Ωστόσο, αυτές οι όγκοι εκφράζονται σε picometer υπερβολικές, ώστε να γίνουν μονάδες angstroms, πολλαπλασιασμού με το συντελεστή μετατροπής (1A / 100 ρΜ)3:
(212,07 μ.μ.3) (1Α / 100pm)3= 2.1207 × 10-4 Α3
(77912297,67 pm3) (1Α / 100pm)3= 77,912 Α3
Έτσι, οι διαφορές στο μέγεθος μεταξύ του μικρού ατόμου του Η και του ογκώδους ατόμου των Cs παραμένουν αριθμητικά εμφανείς. Πρέπει να ληφθεί υπόψη ότι οι υπολογισμοί αυτοί είναι μόνο προσεγγίσεις υπό τον ισχυρισμό ότι ένα άτομο είναι εντελώς σφαιρικό, το οποίο περιπλανιέται μπροστά στην πραγματικότητα.
Παράδειγμα 2

Η πυκνότητα του καθαρού χρυσού είναι 19,32 g / mL και η μοριακή μάζα του είναι 196,97 g / mol. Εφαρμόζοντας τον τύπο M / D για τον υπολογισμό του όγκου ενός mole μορίων χρυσού έχει τα εξής:
VAu= (196,97 g / mol) / (19,32 g / ml) = 10,19 ml / mol
Δηλαδή, 1 mole ατόμων χρυσού καταλαμβάνει 10,19 mL, αλλά τι όγκος κάνει ένα χρυσό άτομο καταλαμβάνουν συγκεκριμένα; Και πώς να το εκφράσετε σε μονάδες pm3? Για το σκοπό αυτό απλά εφαρμόστε τους ακόλουθους συντελεστές μετατροπής:
(10,19 mL / mol) · (mol / 6,02 · 10)-23 (1 m / 100 cm)3· (1 μμ / 10-12m)3= 16,92 · 106 pm3
Από την άλλη πλευρά, η ατομική ακτίνα του χρυσού είναι 166 μμ. Εάν συγκρίνετε και τους δύο όγκους - αυτό που λαμβάνετε με την προηγούμενη μέθοδο και αυτό που υπολογίζεται με τον τύπο του σφαιρικού όγκου - θα διαπιστώσετε ότι δεν έχουν την ίδια τιμή:
VAu= (4/3) (3,14) (166 μm)3= 19,15 · 106 pm3
Ποιο από τα δύο είναι πιο κοντά στην αποδεκτή αξία; Αυτό που είναι πλησιέστερο στα πειραματικά αποτελέσματα που λαμβάνονται με περίθλαση ακτίνων Χ της κρυσταλλικής δομής του χρυσού.
Αναφορές
- Helmenstine, Anne Marie, Ph.D. (09 Δεκεμβρίου 2017). Ατομικός ορισμός έντασης. Ανακτήθηκε στις 6 Ιουνίου 2018, από: thoughtco.com
- Mayfair, Andrew. (13 Μαρτίου 2018). Πώς να υπολογίσετε τον όγκο ενός ατόμου. Sciencing. Ανακτήθηκε στις 6 Ιουνίου 2018, από: sciencing.com
- Wiki Kids Ltd (2018). Lothar Meyer Ατομικές Καμπύλες Όγκου. Ανακτήθηκε στις 6 Ιουνίου 2018, από: wonderwhizkids.com
- Lumen Περιοδικές τάσεις: Ατομικός ακτίνας. Ανακτήθηκε στις 6 Ιουνίου 2018, από: courses.lumenlearning.com
- Camilo J. Derpich. Όγκος και Ατομική Πυκνότητα. Ανακτήθηκε στις 6 Ιουνίου 2018, από: es-puraquimica.weebly.com
- Whitten, Davis, Peck & Stanley. Χημεία (8η έκδοση). CENGAGE Learning, σελ. 222-224.
- CK-12 Foundation. (22 Φεβρουαρίου 2010). Συγκριτικά μεγέθη ατομικών. [Εικόνα] Ανακτήθηκε στις 6 Ιουνίου 2018 από: commons.wikimedia.org
- CK-12 Foundation. (22 Φεβρουαρίου 2010). Ατομική ακτίνα του Η2. [Εικόνα] Ανακτήθηκε στις 6 Ιουνίου 2018 από: commons.wikimedia.org


