Φόρτιση φωσφορικού ασβεστίου (Ca3 (PO4) 2) δομή, ιδιότητες, σχηματισμός και χρήσεις
Το φωσφορικό ασβέστιο είναι ένα ανόργανο και τριτοταγές άλας του οποίου ο χημικός τύπος είναι Ca3(PO4)2. Ο τύπος δηλώνει ότι η σύνθεση αυτού του άλατος είναι 3: 2 για το ασβέστιο και το φωσφορικό, αντίστοιχα. Αυτό μπορείτε να το δείτε απευθείας στην κάτω εικόνα, όπου εμφανίζεται το κατιόν2+ και το PO ανιόν43-. Για κάθε τρία Ca2+ Υπάρχουν δύο PO43- αλληλεπιδρώντας μαζί τους.
Επιπλέον, φωσφορικό ασβέστιο αναφέρεται σε μια σειρά αλάτων ποικίλλουν ανάλογα με την αναλογία Ca / P και του βαθμού ενυδάτωσης και ρΗ. Στην πραγματικότητα, υπάρχουν πολλοί τύποι φωσφορικών ασβεστίου που υπάρχουν και μπορούν να συντεθούν. Ωστόσο, σύμφωνα με την ονοματολογία κυριολεκτικά, το φωσφορικό ασβέστιο αναφέρεται μόνο στο τριασβέστιο, το προαναφερθέν.

Όλα τα φωσφορικά ασβέστιο, συμπεριλαμβανομένου του Ca3(PO4)2, Είναι στερεά λευκά με ελαφριές γκριζωδένες αποχρώσεις. Μπορούν να είναι κοκκώδη, λεπτά, κρυσταλλικά και να έχουν μέγεθος σωματιδίων που είναι γύρω στα μικρόμετρα. και ακόμη και τα νανοσωματίδια αυτών των φωσφορικών έχουν παρασκευαστεί, με τα οποία σχεδιάζονται βιοσυμβατά υλικά για τα οστά.
Αυτή η βιοσυμβατότητα οφείλεται στο γεγονός ότι αυτά τα άλατα βρίσκονται στα δόντια και, εν συντομία, στους ιστούς των οστών των θηλαστικών. Για παράδειγμα, ο υδροξυαπατίτης είναι ένα κρυσταλλικό φωσφορικό ασβέστιο, το οποίο με τη σειρά του αλληλεπιδρά με μια άμορφη φάση του ίδιου άλατος.
Αυτό σημαίνει ότι υπάρχουν άμορφα και κρυσταλλικά φωσφορικά ασβεστίου. Για το λόγο αυτό, η ποικιλομορφία και οι πολλαπλές επιλογές δεν προκαλούν έκπληξη όταν συνθέτουν υλικά με βάση φωσφορικά ασβέστιο. τα υλικά στις ιδιότητες των οποίων οι ερευνητές ενδιαφέρονται περισσότερο καθημερινά παγκοσμίως για να επικεντρωθούν στην αποκατάσταση των οστών.
Ευρετήριο
- 1 Δομή φωσφορικού ασβεστίου
- 1.1 Άμορφο φωσφορικό ασβέστιο
- 1.2 Η υπόλοιπη οικογένεια
- 2 Φυσικές και χημικές ιδιότητες
- 2.1 Ονόματα
- 2.2 Μοριακό βάρος
- 2.3 Φυσική περιγραφή
- 2.4 Γεύση
- 2.5 Σημείο τήξης
- 2.6 Διαλυτότητα
- 2.7 Πυκνότητα
- 2.8 Δείκτης διάθλασης
- 2.9 Πρότυπη ενθαλπία εκπαίδευσης
- 2.10 Θερμοκρασία αποθήκευσης
- 2.11 ρΗ
- 3 Εκπαίδευση
- 3.1 Νιτρικό ασβέστιο και όξινο φωσφορικό αμμώνιο
- 3.2 Υδροξείδιο του ασβεστίου και φωσφορικό οξύ
- 4 Χρήσεις
- 4.1 Στο οστικό ιστό
- 4.2 Βιοκεραμικά τσιμέντα
- 4.3 Γιατροί
- 4.4 Άλλο
- 5 Αναφορές
Δομή φωσφορικού ασβεστίου
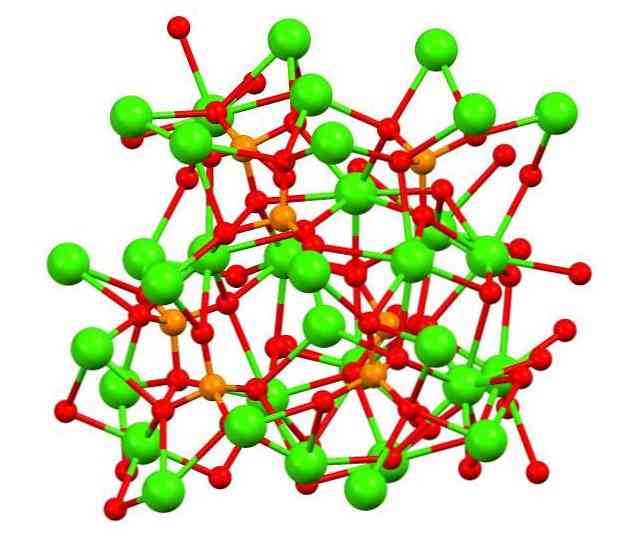
Η επάνω εικόνα δείχνει τη δομή του τριβασικού φωσφορικού καλίου στο περίεργο ορυκτό της ουλοκλείτης, το οποίο μπορεί να περιέχει μαγνήσιο και σίδηρο ως ακαθαρσίες.
Αν και με την πρώτη ματιά μπορεί να φαίνεται πολύπλοκη, είναι απαραίτητο να διευκρινιστεί ότι το μοντέλο υποθέτει ομοιοπολικές αλληλεπιδράσεις μεταξύ των ατόμων οξυγόνου του φωσφορικού και μεταλλικού ασβεστίου κέντρα.
Ως εκπροσώπηση είναι έγκυρη, ωστόσο, οι αλληλεπιδράσεις είναι ηλεκτροστατικές. δηλαδή κατιόντα Ca2+ προσελκύονται από τα ανιόντα PO43- (Ca2+- O-PO33-). Με αυτό κατά νου, είναι κατανοητό γιατί το ασβέστιο εικόνας (πράσινες σφαίρες) περιβάλλονται από άτομα οξυγόνου αρνητικά φορτισμένα (κόκκινες σφαίρες).
Όταν υπάρχουν τόσα ιόντα, δεν αφήνει ορατή συμμετρική διάταξη ή σχέδιο. Το Ca3(PO4)2 Υιοθετεί σε χαμηλές θερμοκρασίες (Τ<1000°C) una celda unitaria correspondiente a un sistema cristalino romboédrico; a este polimorfo se le conoce con el nombre de β-Ca3(PO4)2 (β-TCP, για το ακρωνύμιο της στα αγγλικά).
Σε υψηλές θερμοκρασίες, από την άλλη πλευρά, μετασχηματίζεται στο πολύμορφο α-Ca3(PO4)2 (α-ΤΟΡ), του οποίου το μοναδιαίο κύτταρο αντιστοιχεί σε ένα μονοκλινικό κρυσταλλικό σύστημα. Σε ακόμη υψηλότερες θερμοκρασίες, μπορεί επίσης να σχηματιστεί το πολύμορφο α'-Ca3(PO4)2, που είναι από εξαγωνική κρυσταλλική δομή.
Άμορφο φωσφορικό ασβέστιο
Έχουν αναφερθεί κρυσταλλικές δομές για φωσφορικό ασβέστιο, που αναμένεται από ένα άλας. Ωστόσο, αυτό είναι ικανό να εκδηλώσει διαταραγμένη και ασύμμετρες δομές, που συνδέονται περισσότερο με έναν τύπο «γυαλί φωσφορικού ασβεστίου» ότι οι κρύσταλλοι με την αυστηρή έννοια του ορισμού της.
Όταν συμβαίνει αυτό, λέγεται ότι το φωσφορικό ασβέστιο έχει μια άμορφη δομή (ACP, άμορφο φωσφορικό ασβέστιο). Αρκετοί συγγραφείς υποδεικνύουν αυτόν τον τύπο δομής ως υπεύθυνο για τις βιολογικές ιδιότητες του Ca3(PO4)2 σε ιστούς των οστών, η επισκευή και η βιομιμετοποίησή του είναι δυνατές.
Μέσω της διευκρίνισης της δομής του με πυρηνικό μαγνητικό συντονισμό (NMR), βρέθηκε η παρουσία ιόντων ΟΗ- και HPO42- στην ΑΚΕ. Αυτά τα ιόντα σχηματίζονται με την υδρόλυση ενός από τα φωσφορικά άλατα:
PO43- + H2Ο <=> HPO42- + OH-
Ως αποτέλεσμα, η πραγματική δομή των ΑΚΕ γίνεται πιο πολύπλοκη, η σύνθεση των οποίων αποτελείται από τα εξής: Ca9(PO4)6-χ(HPO4)x(ΟΗ)x. Το «x» δηλώνει το βαθμό ενυδάτωσης, αφού εάν x = 1 τότε ο τύπος θα είναι: Ca9(PO4)5(HPO4) (ΟΗ).
Οι διαφορετικές δομές που η PCA μπορεί να εξαρτάται από τις γραμμομοριακές αναλογίες Ca / P. δηλαδή, των σχετικών ποσοτήτων ασβεστίου και φωσφορικών, οι οποίες αλλάζουν όλη την προκύπτουσα σύνθεση τους.
Η υπόλοιπη οικογένεια
Τα φωσφορικά ασβεστίου είναι στην πραγματικότητα μια οικογένεια ανόργανων ενώσεων, τα οποία με τη σειρά τους μπορούν να αλληλεπιδράσουν με μια οργανική μήτρα.
Τα άλλα φωσφορικά λαμβάνονται "απλά" αλλάζοντας τα ανιόντα που συνοδεύουν το ασβέστιο (PO43-, HPO42-, H2PO4-, OH-), καθώς και τον τύπο ακαθαρσιών στο στερεό. Έτσι, έως και έντεκα φωσφορικά ασβέστιο ή περισσότερα, το καθένα με τη δική του δομή και ιδιότητες, μπορεί να προέρχονται φυσικά ή τεχνητά..
Παρακάτω παρατίθενται ορισμένα φωσφορικά άλατα και οι αντίστοιχες δομές και οι χημικοί τύποι τους:
-Διένυδρο φωσφορικό ασβέστιο υδρογόνου, CaHPO4∙ 2H2Ο: μονοκλινική.
-Μονοϋδρικό φωσφορικό δισόξινο ασβέστιο, Ca (H)2PO4)2∙ H2Ο: τρικλινικό.
-Άνυδρο φωσφορικό διοξείδιο, Ca (H)2PO4)2: τρικλίνικα.
-Οξικό φωσφορικό ασβέστιο (OCP), Ca8H2(PO4)6: τρικλίνικα Είναι πρόδρομος στη σύνθεση του υδροξυαπατίτη.
-Υδροξυαπατίτης, Ca5(PO4)3OH: εξαγωνικό.
Φυσικές και χημικές ιδιότητες
Ονόματα
-Φωσφορικό ασβέστιο
-Φωσφορικό ασβέστιο
-Διφωσφορικό τριασβέστιο
Μοριακό βάρος
310,74 g / mol.
Φυσική περιγραφή
Είναι άοσμο λευκό στερεό.
Γεύση
Ασταμάτητο.
Σημείο τήξης
1670 º Κ (1391 ºC).
Διαλυτότητα
-Πρακτικά αδιάλυτο στο νερό.
-Αδιάλυτο σε αιθανόλη.
-Διαλυτό σε αραιό υδροχλωρικό οξύ και νιτρικό οξύ.
Πυκνότητα
3,14 g / cm3.
Δείκτης διάθλασης
1,629
Τυπική ενθαλπία κατάρτισης
4126 kcal / mol.
Θερμοκρασία αποθήκευσης
2-8 ºC.
ρΗ
6-8 σε ένα υδατικό εναιώρημα 50 g / L φωσφορικού ασβεστίου.
Εκπαίδευση
Νιτρικό ασβέστιο και φωσφορικό αμμώνιο υδρογόνου
Υπάρχουν πολλές μέθοδοι για την παραγωγή ή τη διαμόρφωση φωσφορικού ασβεστίου. Ένα από αυτά αποτελείται από ένα μίγμα δύο αλάτων, Ca (NO)3)2∙ 4Η2Ο και (ΝΗ4)2HPO4, προηγουμένως διαλυμένα σε απόλυτη αλκοόλη και νερό, αντίστοιχα. Ένα άλας παρέχει ασβέστιο και το άλλο φωσφορικό.
Από αυτό το μίγμα κατακρημνίζονται τα ΑΟΡ, τα οποία κατόπιν υποβάλλονται σε θέρμανση σε κλίβανο στους 800 ° C και για 2 ώρες. Ως αποτέλεσμα αυτής της διαδικασίας, λαμβάνεται β-Ca3(PO4)2. Με τον προσεκτικό έλεγχο των θερμοκρασιών, της ανάδευσης και των χρόνων επαφής μπορεί να προκύψει σχηματισμός νανοκρυστάλλων.
Για τον σχηματισμό του πολύμορφου α-Ca3(PO4)2 είναι απαραίτητο να θερμανθεί το φωσφορικό πάνω από 1000 ° C. Αυτή η θέρμανση διεξάγεται παρουσία άλλων μεταλλικών ιόντων, τα οποία σταθεροποιούν αυτό το πολύμορφο επαρκώς ώστε να χρησιμοποιηθούν σε θερμοκρασία δωματίου. δηλαδή, παραμένει σε μια σταθερή μετα-κατάσταση.
Υδροξείδιο ασβεστίου και φωσφορικό οξύ
Το φωσφορικό ασβέστιο μπορεί επίσης να σχηματιστεί με ανάμιξη των διαλυμάτων του υδροξειδίου του ασβεστίου και του φωσφορικού οξέος, με την εξουδετέρωση της όξινης βάσης. Μετά από μισή ημέρα ωρίμανσης σε μητρικά υγρά, και κατάλληλο φιλτράρισμα του, πλύσιμο, ξήρανση και κοσκίνισμα, μια κοκκώδης σκόνη του άμορφου φωσφορικού λαμβάνεται, ΑΚΕ.
Αυτό το αντιδραστικό προϊόν ΑΚΕ υψηλών θερμοκρασιών, που μετασχηματίζεται σύμφωνα με τις ακόλουθες χημικές εξισώσεις:
2Ca9(HPO4) (PO4)5(ΟΗ) => 2Ca9(Ρ2Ο7)0,5(PO4)5(ΟΗ) + Η2Ο (σε Τ = 446,60 ° C)
2Ca9(Ρ2Ο7)0,5(PO4)5(ΟΗ) => 3Ca3(PO4)2 + 0.5Η2Ο (σε Τ = 748,56 ° C)
Με αυτόν τον τρόπο, λαμβάνεται β-Ca3(PO4)2, το πιο κοινό και σταθερό πολύμορφο.
Χρησιμοποιεί
Στο οστικό ιστό
Το Ca3(PO4)2 Είναι το κύριο ανόργανο συστατικό της τέφρας των οστών. Είναι ένα συστατικό των μεταμοσχεύσεων οστικής αντικατάστασης, εξηγείται από τη χημική του ομοιότητα με τα ορυκτά που υπάρχουν στο οστό.
Τα βιοϋλικά του φωσφορικού ασβεστίου χρησιμοποιούνται για τη διόρθωση των οστικών ελαττωμάτων και στην επικάλυψη προθέσεων μετάλλου τιτανίου. Το φωσφορικό ασβέστιο εναποτίθεται πάνω τους, απομονώντας τα από το περιβάλλον και επιβραδύνοντας τη διαδικασία διάβρωσης του τιτανίου.
Φωσφορικά ασβεστίου, συμπεριλαμβανομένου του Ca3(PO4)2, Χρησιμοποιούνται για την παραγωγή κεραμικών υλικών. Αυτά τα υλικά είναι βιοσυμβατά, και χρησιμοποιούνται επί του παρόντος για την αποκατάσταση της απώλειας φατνιακού οστού που προκύπτει από περιοδοντική νόσο, ενδοδοντική λοιμώξεις και άλλες συνθήκες.
Ωστόσο, θα πρέπει να χρησιμοποιούνται μόνο για την επιτάχυνση της αποκατάστασης των περιασικών οστών, σε περιοχές όπου δεν υπάρχει χρόνια βακτηριακή λοίμωξη.
Το φωσφορικό ασβέστιο μπορεί να χρησιμοποιηθεί στην αποκατάσταση ελαττωμάτων οστού, όταν δεν είναι δυνατόν να χρησιμοποιηθεί ένα αυτογενές οστικό μόσχευμα. Είναι δυνατόν να χρησιμοποιηθεί μόνη της ή σε συνδυασμό με ένα βιοαποικοδομήσιμο και αναρροφήσιμο πολυμερές, όπως το πολυγλυκολικό οξύ.
Βιοκεραμικά τσιμέντα
Το τσιμέντο φωσφορικού ασβεστίου (CPC) είναι ένα άλλο βιοκεραμικό που χρησιμοποιείται στην επιδιόρθωση οστικού ιστού. Δημιουργείται με ανάμιξη της σκόνης διαφόρων τύπων φωσφορικών ασβεστίου με νερό, σχηματίζοντας μια πάστα. Η πάστα μπορεί να εγχυθεί ή να προσαρμοσθεί στο ελάττωμα οστού ή στην κοιλότητα.
Τα τσιμέντα χυτεύονται, βαθμιαία απορροφούνται και αντικαθίστανται από νεοσχηματισμένο οστό.
Γιατροί
-Το Ca3(PO4)2 Είναι ένα βασικό άλας, επομένως χρησιμοποιείται ως αντιόξινο για να εξουδετερώνει το υπερβολικό οξύ του στομάχου και να αυξάνει το pH. Στην οδοντόκρεμα, παρέχει μια πηγή ασβεστίου και φωσφορικών για τη διευκόλυνση της διαδικασίας αναμικροποίησης των οδόντων και οστικής αιμόστασης.
-Χρησιμοποιείται επίσης ως συμπλήρωμα διατροφής, αν και ο φθηνότερος τρόπος αντικατάστασης του ασβεστίου είναι η χρήση του ανθρακικού και κιτρικού του..
-Το φωσφορικό ασβέστιο μπορεί να χρησιμοποιηθεί στη θεραπεία της τετανίας, της λανθάνουσας υποαλκαιμίας και της θεραπείας συντήρησης. Επιπλέον, είναι χρήσιμο στο συμπλήρωμα ασβεστίου κατά τη διάρκεια της εγκυμοσύνης και του θηλασμού.
-Χρησιμοποιείται για τη θεραπεία μιας μόλυνσης με ραδιενεργό ισότοπο ραδιόφωνο (Ra-226) και στροντίου (Sr-90). Το φωσφορικό ασβέστιο εμποδίζει την απορρόφηση ραδιενεργών ισότοπων στο πεπτικό σύστημα, περιορίζοντας έτσι τη ζημία που προκαλείται από αυτά.
Άλλοι
-Το φωσφορικό ασβέστιο χρησιμοποιείται ως τροφή για πτηνά. Επιπλέον, χρησιμοποιείται στις οδοντόκρεμες για τον έλεγχο της πέτρας.
-Χρησιμοποιείται ως αντιπηκτικό μέσο, για παράδειγμα για να αποφευχθεί η συμπύκνωση του επιτραπέζιου αλατιού.
-Λειτουργεί ως λευκαντικό για το αλεύρι. Ενώ, στο λαρδί χοίρου αποτρέπει ανεπιθύμητο χρωματισμό και βελτιώνει την κατάσταση του τηγανίσματος.
Αναφορές
- Tung M.S. (1998) Φωσφορικά ασβέστιο: δομή, σύνθεση, διαλυτότητα και σταθερότητα. Στο: Amjad Ζ. (Eds) Φωσφορικά ασβεστίου σε βιολογικά και βιομηχανικά συστήματα. Springer, Βοστώνη, ΜΑ.
- Langlang Liu, Yanzeng Wu, Chao Xu, Suchun Yu, Xiaopei Wu και Honglian Dai. (2018). «Σύνθεση, χαρακτηρισμός φωσφορικού νανο-β-τριασβεστίου και αναστολή κυττάρων καρκινώματος του ήπατος», Journal of Nanomaterials, τομ. 2018, αρ. Ταυτ. 7083416, 7 σελίδες, 2018.
- Combes, Χριστός και Rey, Χριστιανός. (2010). Άμορφα φωσφορικά ασβέστιο: σύνθεση, ιδιότητες και χρήσεις σε βιοϋλικά. Acta Biomaterialia, νοΙ. 6 (n ° 9). σ. 3362-3378. ISSN 1742-7061
- Wikipedia. (2019). Φωσφορικό ασβέστιο. Ανακτήθηκε από: en.wikipedia.org
- Abida et αϊ. (2017). Πούδρα φωσφορικού ασβεστίου: Προετοιμασία, χαρακτηρισμός και συμπύκνωση. Μεσογειακή Εφημερίδα της Χημείας 2017, 6 (3), 71-76.
- PubChem. (2019). Φωσφορικό ασβέστιο. Ανακτήθηκε από: pubchem.ncbi.nlm.nih.gov
- Elsevier (2019). Φωσφορικό ασβέστιο. Science Direct. Ανακτήθηκε από: sciencedirect.com


